ไฟโคไซยานิน
ไฟโคไซยานิน
ชื่อสามัญ Phycocyanin
ประเภทและข้อแตกต่างไฟโคไซยานิน
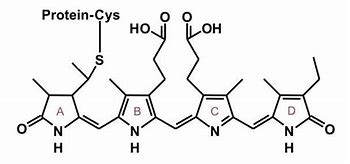
ไฟโคไซยานิน คือ ไฟโคบิลิโปรตีนหนึ่ง ซึ่งเป็นรงควัตถุที่มีสีน้ำเงิน หรือ เป็นสารประกอบที่มีสีฟ้าเรืองแสงได้ และสามารถละลายน้ำได้ โดยทั่วไป ไฟโคไซยานินจะให้ค่าการดูดกลืนแสงสูงสุด (λmax) ในช่วงความยาวคลื่น 610 ถึง 620 นาโนเมตร และเมื่อเรืองแสงจะวัดค่าการดูดกลืนแสงสูงสุดได้ที่ช่วงความยาวคลื่น 636 ถึง 650 นาโนเมตร ส่วนโมเลกุลของไฟโคไซยานิน จะรวมตัวอยู่ในรูปไตรเมอร์ (α3β3) เฮกซะเมอร์ (α6β6) และโอลิโกเมอร์ (Oligomers) แบบอื่นๆ สารประกอบเชิงซ้อนเหล่านี้ก่อตัวขึ้นจากโมโนเมอร์ (αβ-monomer) ของไฟโคไซยานิน ซึ่งประกอบด้วย หน่วยย่อยอัลฟา (α-subunit) และหน่วยย่อยเบต้า (β-subunit) โดยที่หน่วยย่อยอัลฟา และหน่วยย่อยเบต้าดังกล่าวแต่ละหน่วยจะมีใบลินเกาะอยู่กับกรดอะมิโนซิสเตอีนบนอะโพโปรตีนของหน่วยย่อย 1 และ 2 หมู่ตามลำดับ
สำหรับประเภทของไฟโคไซอินนั้นสามารถแบ่งออกเป็น 2 ประเภท ตามสัญลักษณ์ หรือ การเขียนชื่อของไฟโคไซยานิน ซึ่งโดยทั่วไปมักใช้คำนำหน้า (Prefix) ของคำว่า Phycocyanin เช่น C- หรือ R- เพื่อบอกถึงเหล่าที่มาของสารประกอบนั้นที่ค้นพบเป็นครั้งแรก โดยไฟโคไซยานินที่พบมาก คือ C-Phycocyanin ซึ่งเป็นไฟโคไซยานินที่พบในไซยาโนแบคทีเรีย ส่วน R-Phycocyanin เป็นไฟโคไซยานินที่พบในสาหร่ายสีแดงในคลาส Rhodophyceae เป็นต้น
แหล่งที่พบและแหล่งที่มาไฟโคไซยานิน
ไฟโคไซยานินเป็นรงควัตถุ หรือ สารประกอบที่ได้จากกระบวนการสังเคราะห์ และสกัดจากสาหร่ายสีเขียวแกมน้ำเงินทุกชนิด สาหร่ายสีแดง และสาหน่ายสีทอง บางชนิด อาทิ เช่น Spirulina sp., Phormidium sp., Lyngbya sp., Anacystis nidulans, Spirulina (Arthrospira) fusiformis, Thermosynechcoccus vulcanus, Porphyridium cruentum เป็นต้น
ทั้งนี้สาหร่ายที่เป็นแหล่งที่มาของไฟโคไซยานิน อาจมีคุณสมบัติในการต้านอนุมูลอิสระ และค่าการดูดกลิ่นแสงที่ต่างกันได้ โดยจะขึ้นอยู่กับประเภท-สปีชี่ของสาหร่าย แหล่งที่มาวิธีการเพาะเลี้ยงวิธีการสกัดออกจากเซลล์และกระบวนการหลังการสกัด เป็นต้น

ปริมาณที่ควรได้รับจากไฟโคไซยานิน
ในปัจจุบันยังไม่มีการกำหนดเกณฑ์ และรูปแบบการใช้ไฟโคไซยานิน ที่แน่ชัดเหมือนกับการกำหนดเกณฑ์ของปริมาณสารอาหารที่ควรได้รับประจำวัน เพราะไฟโคไซยานินไม่ได้เป็นสารอาหารที่จำเป็นต่อร่างกายโดยเป็นเพียงสารที่ใช้ในการป้องกันการเกิดภาวะการเจ็บป่วยบางประการ ของร่างกายเท่านั้น ซึ่งในปัจจุบันได้มีการสกัดไฟโคไซยานินจากสาหร่ายมาใช้เป็นผลิตภัณฑ์เสริมอาหารวางจำหน่ายตามร้านค้าต่างๆ มากมาย ดังนั้นในการใช้ผลิตภัณฑ์เสริมอาหารดังกล่าวจึงควรปรึกษาแพทย์ผู้เชี่ยวชาญก่อนใช้ทุกครั้ง เพื่อความปลอดภัยจากผลข้างเคียงทั้งในระยะสั้นและระยะยาว
ประโยชน์และโทษไฟโคไซยานิน
สำหรับประโยชน์ของไฟโคไซยานิน นั้น จากการศึกษาพบว่าไฟโคไซยานินมีประโยชน์อย่างมากในทางอุตสาหกรรม และเภสัชกรรม โดยเฉพาะคุณสมบัติของรงควัตถุที่ทำให้เกิดสีในสาหร่ายจึงมีการนำไปใช้ในโรงงานอุตสาหกรรม เพื่อเป็นสารแต่งสีจากธรรมชาติแทนการใช้สารแต่งสีสังเคราะห์ในอุตสาหกรรมอาหาร และเครื่องสำอาง อาทิ ไอศกรีม เจลลี่ลูกกวาด อายไลน์เนอร์ และลิปสติก เป็นต้น
นอกจากนี้ในทางเภสัชกรรม และทางการแพทย์ยังมีการศึกษาวิจัยสารไฟโคไซยานิน พบว่ามีฤทธิ์ต้านอนุมูลอิสระ (antioxidant) ต้านการอักเสบ (anti-inflammatory) และช่วยป้องกันเซลล์สมองไม่ให้ถูกทำลาย (neuroprotective) ได้ ดังนั้นในปัจจุบันจึงมีการสกัดไฟโคไซยานินจากสาหร่ายมาใช้เป็นผลิตภัณฑ์เสริมอาหารเพื่อป้องกันการเกิดอนุมูลอิสระที่เป็นสาเหตุของโรคมะเร็ง อัลไซเมอร์ ภาวะแก่ก่อนวัย โดยหัวใจ และหลอดเลือด รวมถึงการอักเสบต่างๆ ของร่างกายโดยการสกัดไฟโคไซยานินในปัจจุบันอาศัยหลักการทำลายผนังเซลล์เพื่อให้ไฟโคไซยานินซึ่งเป็นส่วนหนึ่งของเยื่อไทลาคอยด์จะถูกปลดปล่อยออกสู่ภายนอกเซลล์ โดยสามารถทำได้หลายวิธี แต่สามารถแบ่งได้เป็น 3 ประเภท คือ (1) การใช้แรงกล เช่น เครื่องบด คลื่นอัลตราโซนิก และการใช้แรงดันสูง (2) การทำลายทางกายภาพ เช่น ความร้อน หรือ การแช่เยือกแข็งสลับกับการละลาย และ (3) การย่อยด้วยเอนไซม์ หรือ สารเคมี อย่างไรก็ตาม วิธีที่เหมาะสมที่ใช้ในการสกัดไฟโคไซยานิน ในสาหร่ายแต่ละชนิดจะมีความแตกต่างกัน และปริมาณของไฟโคไซยามินก็จะแตกต่างกันเช่นกัน
การศึกษาวิจัยที่เกี่ยวข้องไฟโคไซยานิน
มีผลการศึกษาวิจัยถึงคุณสมบัติของไฟโคไซยานินด้านการแพทย์พบว่ามีฤทธิ์ต่างๆ ดังนี้
ฤทธิ์ต้านอนุมูลอิสระ จาการศึกษาวิจัยพบว่าสารไฟโคไซยานินมีความสามารถในการกำจัดอนุมูลไฮดรอกซิล (Hydroxyl radicals) และอนุมูลเปอร์ออกซิล (Peroxyl radical) โดยมีไฟโคไซยาโนไบลินทำหน้าที่ในการต้านการเกิดปฏิกิริยาออกซิเดชั่น และกำจัดอนุมูลอิสระ โดยไฟโคไซยานินที่สกัดจากสาหร่าย Aphanizomenon flos-aquae (AFA) ซึ่งอยู่ในกลุ่มไซยาโนแบคทีเรียมีความสามารถกําจัดอนุมูลเปอร์ออกซิลได้เช่นเดียวกัน และยังพบว่าไฟโคไซยานินจากสาหร่าย S. platensis จะสร้างอนุมูลไฮดรอกซิลในสภาวะที่มีแสง แต่จะกำจัดอนุมูลโฮดรอกซิลในสภาวะที่ไม่มีแสง การทําให้ไฟโคไซยานินเสียสภาพทางธรรมชาติโดยใช้สารเคมีจะทำให้ความสามารถในการสร้างอนุมูลดังกล่าวหมดไป และในทางตรงกันข้ามไฟโคไซยานินที่สูญเสียสภาพทางธรรมชาติจะมีความสามารถในการกำจัดอนุมูลโฮดรอกซิลเพิ่มขึ้น ซึ่งชี้ว่าไฟโคไซยาโนไบลินทำหน้าที่หลักในการกำจัดอนุมูลโฮดรอกซิล และพบว่าส่วนของอะโพโปรตีนก็มีคุณสมบัตินี้ด้วยเช่นเดียวกัน ความสามารถในการกำจัดอนุมูลไฮดรอกซิลดังกล่าวยังเพิ่มขึ้นตามความเข้มข้นของไฟโคไซยานินที่เพิ่มขึ้นอีกด้วย
และยังมีอีกการศึกษาหนึ่งพบว่าซี-ไฟโคไซยานิน (C-phycocyanin) มีคุณสมบัติที่สามารถกำจัดสารอนุมูลอิสระได้ โดยการสร้างพันธะ หรือ ให้อิเล็กตรอนกับโมเลกุลที่เป็นอนุมูลอิสระ เช่น อนุมูลอิสระแอลคอกซี (alkoxy radical) อนุมูลอิสระไฮดรอกซี (hydroxyl radical) อนุมูลอิสระเปอร์ออกซี (peroxyl radical) อนุมูลอิสระเปอร์ออกซีไนไตรท (peroxinitrite) อนุมูลอิสระ DPPH และอนุมูลอิสระ ABTS เป็นต้น ส่งผลให้เกิดความเสถียรของอิเล็กตรอนช่วยปกป้องและลดความรุนแรงจากการทำปฏิกิริยาของอนุมูลอิสระภายในเซลล์ได้ส่วนศึกษาสมบัติการต้านอนุมูลอิสระของซี-ไฟโคไซยานิน (C-phycocyanin) ที่สกัดได้จากไซยาโนแบคทีเรีย 3 ชนิด ได้แก่Lyngbya sp., Phormidium sp. และ Spirulina sp. พบว่าสามารถต้านอนุมูลอิสระเปอร์ออกซี และอนุมูลอิสระไฮดรอกซีได้ โดยซี-ไฟโคไซยานินที่ได้จาก Phormidium sp. สามารถต้านอนุมูลอิสระไฮดรอกซีได้ดีกว่าซี-ไฟโคไซยานินจาก Lyngbya sp. และ Spirulina sp. ตามลำดับ และพบว่าซี-ไฟโคไซยานินที่ได้จาก Lyngbya sp. สามารถต้านอนุมูลอิสระเปอร์ออกซีได้ดีกว่า Spirulina sp. และ Phormidium sp. ตามลำดับ
ฤทธิ์ต้านอักเสบมีการรายงานว่าซี-ไฟโคไซยานิน (C-phycocyanin) สามารถยับยั้ง และชะลอการก่อตัวของสาร iNOS (inducible nitric oxide synthase) COX-2 (Cyclooxygenase-2) PGE2 (prostaglandin E2) และสารที่ชักนำให้เกิดเนื้อร้าย TNFa (tumornecrosis factor-a) อีกทั้งยังลดการแทรกซึมของนิวโทรฟิล (neutrophil) ซึ่งถูกเหนี่ยวนำด้วยสารคาราจีแนนบริเวณอุ้งเท้าหนูได้โดยสารดังกล่าวนี้ เป็นสาเหตุที่ส่งผลให้เกิดการอักเสบ และความเจ็บปวด
ฤทธิ์ปกป้องเซลล์ประสาท มีการศึกษาบทบาทของ ซี-ไฟโคไซยานิน ในการปกป้องเซลล์ประสาทหนูโดยชักนำให้เซลล์สมองหนูเกิดการตายโดยการขาดโพแทสเซียม และซีรัม (K/S) ส่งผลให้เกิดภาวะออกซิเดชันเกินสมดุล พบว่า ซี-ไฟโคไซยานิน สามารถป้องกันการตายของเซลล์สมองหนูได้ซึ่งอาจเกิดจากการยับยั้งการก่อตัวของสารอนุมูลอิสระที่ส่งผลทำลายเซลล์ประสาทของหนู
นอกจากนี้ในกระบวนการผลิต และสกัดไฟโคไซยานินยังมีผลการศึกษาวิจัยระบุว่าการสังเคราะห์พิกเมนต์กลุ่มไฟโคบิลิโปรตีนของสาหร่ายจะตอบสนองได้ดีต่อการเหนี่ยวนำทางสิ่งแวดล้อม โดยเฉพาะคุณภาพแสง โดยพบว่าสภาวะของแสงและอุณหภูมิที่เหมาะสมต่อการผลิตไฟโคบิลิโปรตีนของสาหร่าย Spirulina platensis ในการเลี้ยงแบบคราวเดียว คือ ที่ 2,000 lux และที่ 35 องศาเซลเซียส ส่วนอีกการศึกษาหนึ่งพบว่าเซลล์ของสาหร่ายสดจะให้ผลผลิตไฟโคไซยานินสูงกว่าการใช้เซลล์แห้ง โดยที่การทำแห้งสาหร่ายสไปรูไลนาด้วยวิธีต่างๆ กัน เช่น การทำแห้งด้วยเครื่องทำแห้งแบบพ่นฝอย และการทำแห้งด้วยตู้อบลมร้อนจะสูญเสียไฟโคไซยานินถึงร้อยละ 45 เมื่อเทียบกับการใช้เซลล์สด
ข้อแนะนำและข้อควรปฏิบัติ
มีรายงานการศึกษาวิจัยเกี่ยวกับการผลิตทางการค้าของไฟโคไซยานิน กล่าวว่าไฟโคไซยานินที่ใช้ในอุตสาหกรรมยาต้องใช้ชนิดที่มีความบริสุทธิ์ 4.0 ส่วน ชนิดที่ใช้ในอุตสาหกรรมอาหารต้องใช้ชนิดที่มีความบริสุทธิ์ 2.0 ดังนั้นในการเลือกผลิตภัณฑ์เสริมอาหารจากไฟโคไซยานินจึงควรสอบถาม หรือ สืบค้นของแหล่งที่มา แหล่งผลิต รวมถึงความบริสุทธิ์ของวัตถุดิบ และสารสกัดที่นำมาใช้ผลิต นอกจากนี้ในการใช้ผลิตภัณฑ์เสริมอาหาร เนื่องจากยังไม่มีเกณฑ์ และข้อกำหนดในการใช้ที่แน่ชัด อีกทั้งขนาด และปริมาณในการใช้ก็ยังไม่มีข้อมูลที่แน่นอน ดังนั้นก่อนการใช้จึงควรต้องปรึกษาแพทย์ผู้เชี่ยวชาญก่อนใช้เสมอ
เอกสารอ้างอิง ไฟโคไซยานิน
- วันเพ็ญ ภูติจันทร์. 2549. วิทยาสาหร่าย. โอ เอส พริ้นติ้ง เฮาส์, กรุงเทพฯ.
- รชนิมุข หิรัญส่งจาเลิศ, กนกนันท์ เอกบรรพต, มะลิวัลย์ คุตะโก, ศรีสมาน ธาระนาถ. ผลของความเข้มแสงต่อปริมาณ ซี-ไฟโคไซยานิน ในส่าหร่าย. วารสารแก่นเกษตรปีที่ 43. ฉบับพิเศษ 1. 2558. หน้า 548-555
- ราเชนทร์ ดวงศรี. 2552. การสกัด และความคงตัวของไฟโคไซยานิน จากสาหร่ายสไปรูไลนา. วิทยานิพนธ์ปริญญาวิทยาศาสตรมหาบัณฑิต, สาขาเทคโนโลยีอาหาร, มหาวิทยาลัยเทคโนโลยีสุรนาร
- Bhat, V. B. and Madyastha, K. M. (2000). C-Phycocyanin: A potent peroxyl radical scavenger in vivo and in vitro .Biochemical and Biophysical Research Communications. 275: 20- 25.
- Romay, C., Gonzalez, R., Ledon, N., Remirez, D., & Rimbau, V. (2003). C-Phycocyanin: a biliprotein with antioxidant, anti-inflammatory and neuroprotective effects. Current Protein and Peptide Science, 4(3), 207-216
- Glazer, A.N. and Hixson, C.S. (1975). Characterization of R-Phycocyanin: chromophore content of R-Phycocyanin and C-Phycoerytrin. J. Biological Chemistry. 250(14): 5487-5495
- Patel, A., Mishra, S., & Ghosh, P. K. (2006). Antioxidant potential of C-phycocyanin isolated from cyanobacterial species Lyngbya, Phormidium and Spirulina spp. Indian Journal of Biochemistry and Biophysics, 43(1), 25-31.
- Bhaskar, S.U., Gopalaswamy, G. and Raghu, R. A. (2005). Simple method for efficient extraction and purification of C-Phycocyanin from Spirulina platensis Geitler. Indian J. Experimental Biology. 43(3): 277-279.
- Shih, C. M., Cheng, S. N., Wong, C. S., Kuo, Y. L., & Chou, T. C. (2009). Antiinflammatory and antihyperalgesic activity of C-phycocyanin. Anesthesia and Analgesia, 108(4), 1303-1310
- Benedetti, S., Benvenuti, F., Pagliarani, S., Francogli, S., Scoglio, S. and Canestrari, F. (2004). Antioxidant properties of a novel phycocyanin extract from the blue-green alga Aphanizomenon flos-aquae. Life Sciences. 75: 2353–2362.
- Fukui, K., Saito, T., Noguchia, Y., Kodera, Y., Matsushimaa, A., Nishimura, H. and Inada, Y. (2004). Relationship between color development and protein conformation in the PC molecule. Dyes and Pigments. 63: 89-94.
- Sarada, R., Pillai, M. G. and Ravishankar, G.A. (1999). Phycocyanin from Spirulina sp: influence of processing of biomass on phycocyanin yield, analysis of efficacy of extraction methods and stability studies on phycocyanin. Process Biochemistry. 34: 795–801
- Chorus, I. and Bartram, J. 1999. Toxic cyanobacteria in water: A guide to their public health consequences monitoring and management. St Edmundsbury Press, New York.
- Bhat, V. B. and Madyastha, K. M. (2001). Scavenging of peroxynitrite by phycocyanin and phycocyanobilin from Spirulina platensis: Protection against oxidative damage to DNA. Biochemical and Biophysical Research Communications. 285: 262–266.
- Rimbau, V., Camins, A., Pubill, D., Sureda, F. X., Romay, C., Gonzalez, R., Jiménez, A., Escubedo, E., Camarasa, J., & Pallàs, M. (2001). C-Phycocyanin protects cerebellar granule cells from low potassium/serum deprivation-induced apoptosis. Naunyn-Schmiedeberg's Archives of Pharmacology, 364(2), 96-104.
- Adir, N. and Lerner, N. (2003). The crystal structure of a novel unmethylated form of C-Phycocyanin, a possible connector between cores and rods in phycobilisomes. J. Bio Chem .278(28): 25926-25932.
- Estrada, J.E.P., Bescos, P.B. and Fresno, A.M.V.D. (2001). Antioxidant activity of different fractions of Spirulina platensis protean extract. Il Farmaco. 56: 497–500.