ธาตุเหล็ก
ธาตุเหล็ก
ชื่อสามัญ Iron
ประเภทและข้อแตกต่างธาตุเหล็ก
ธาตุเหล็กเป็นเกลือแร่ชนิดหนึ่ง ที่มีความจำเป็นต่อร่างกายเป็นอย่างยิ่ง โดยเป็นส่วนประกอบสำคัญของโปรตีนที่นำออกซิเจน เช่น ฮีโมโกลบินซึ่งอยู่ในเม็ดเลือดแดง ไมโอโกลบิน ซึ่งอยู่ในกล้ามเนื้อ สำหรับประเภทของธาตุเหล็ก นั้นสามารถแบกออกได้เป็น 2 ประเภท ตามรูปแบบในอาหาร ได้แก่ ธาตุเหล็กที่อยู่ในรูป heme ซึ่งเป็นองค์ประกอบของฮีโมโกลบิน และมัยโอโกลบิน ส่วนอีกประเภทหนึ่ง คือ ธาตุเหล็กที่อยู่ในรูปของ inorganic iron หรือ ferritin ที่เรียกว่าเป็น non-heme iron ซึ่งความแตกต่างของรูปแบบทั้ง 2 กลุ่มนี้ คือ ธาตุเหล็กในรูปแบบ heme จะสามารถดูดซึมไปใช้ได้โดยตรง และมักจะดูดซึมได้สูง ส่วนรูปแบบ none-heme –iron การดูดซึมจะมีปัจจัยส่งเสริมหรือขัดขวางจากอาหารอื่นๆ เข้ามาเกี่ยวข้อง และดูดซึมได้น้อย
แหล่งที่พบและแหล่งที่มาธาตุเหล็ก
โดยปกติแล้วในร่างกายมนุษย์จะมีธาตุเหล็ก อยู่ประมาณ 40-50 มก./นน. ตัว 1 กก. (หรือประมาณ 2-4 กรัม ของเหล็ก) โดยร้อยละ 60-70 ของธาตุเหล็กในร่างกายจะอยู่ในฮีโมโกบิน (hemoglobin) ในเม็ดเลือดแดง [red blood cell (RBC)] ส่วนที่เหลือจะถูกเก็บสะสมในตับและม้าม ในรูปของ ferritin และ hemosiderin ซึ่งปริมาณดังกล่าวอาจยังไม่เพียงพอต่อความต้องการของร่างกาย ดังนั้นร่างกายจึงควรได้รับ ธาตุเหล็กจากอาหารต่างๆ โดยอาหารที่เป็นแหล่งของธาตุเหล็กสามารถแยกตามกลุ่มโครงสร้าง หรือ ประเภทของธาตุเหล็ก ได้ดังนี้

กลุ่มอาหารที่มีธาตุเหล็ก ที่อยู่ในรูป heme มักจะได้จากแหล่งเนื้อสัตว์ และเครื่องในสัตว์ ซึ่งแหล่งอาหารที่เป็นเนื้อสัตว์ ตับ เครื่องใน มีธาตุเหล็กในรูปของ heme ประมาณร้อยละ 30-50 เลือดหมู เลือดไก่มีธาตุเหล็กทั้งหมด ส่วนอาหารทะเล เช่น กุ้ง ปลาหมึก มีธาตุเหล็ก รูป heme ร้อยละ 1-10 หอยบางชนิดมีธาตุเหล็กโดยรวม และสัดส่วนที่เป็นรูป heme สูงใกล้เคียงกับกลุ่มเครื่องใน และเนื้อแดง ส่วนเนื้อเป็ด ไก่ และปลา มีทั้งที่มี heme สูง ได้แก่ส่วนของเนื้อสีคล้ำ เช่น ส่วนอกของเป็ด ไก่ และปลา ส่วนใหญ่ มี heme อยู่เพียงร้อยละ 10-15 ซึ่งอาหารในกลุ่มนี้ คือ เป็นแหล่งอาหารชั้นดีที่มีธาตุเหล็กสูง ส่วนอีกกลุ่มหนึ่ง คือ อาหารพวกพืชต่างๆ ได้แก่ ธัญพืช ต่างๆ รวมทั้ง ข้าว ถั่วเมล็ดแห้ง และถั่วเหลือง รวมถึงใน ผักต่างๆ ผักเขียวเข้ม อยู่ในรูป non-heme รวมทั้งธาตุเหล็กในน้ำนมวัว และไข่ แม้จะเป็นกลุ่มเนื้อสัตว์แต่อยู่ในรูป non-heme เช่นกัน

แหล่งอาหารธาตุเหล็กชนิดไม่ใช่ฮีม (ดูดซึมร้อยละ 3-5)
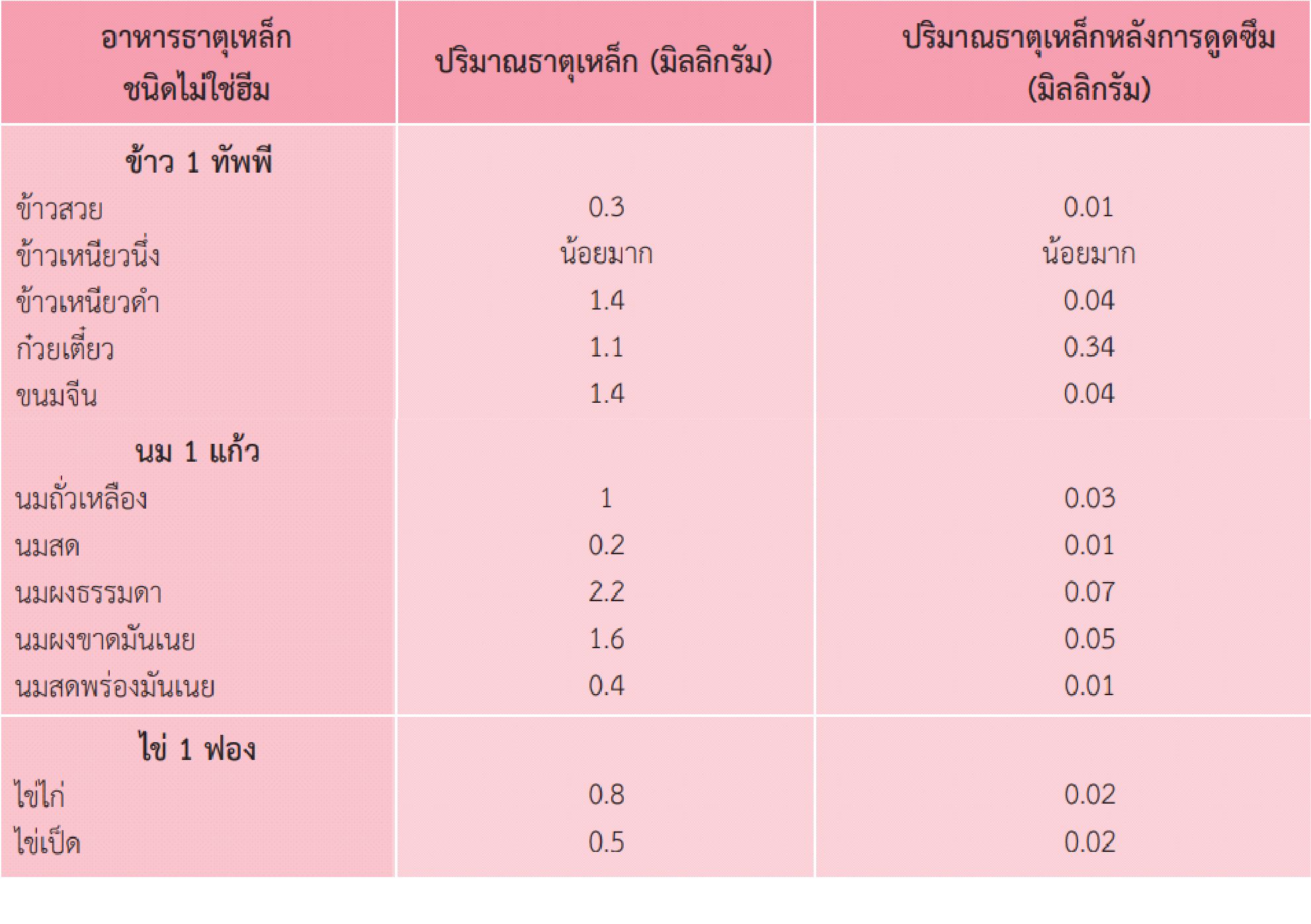
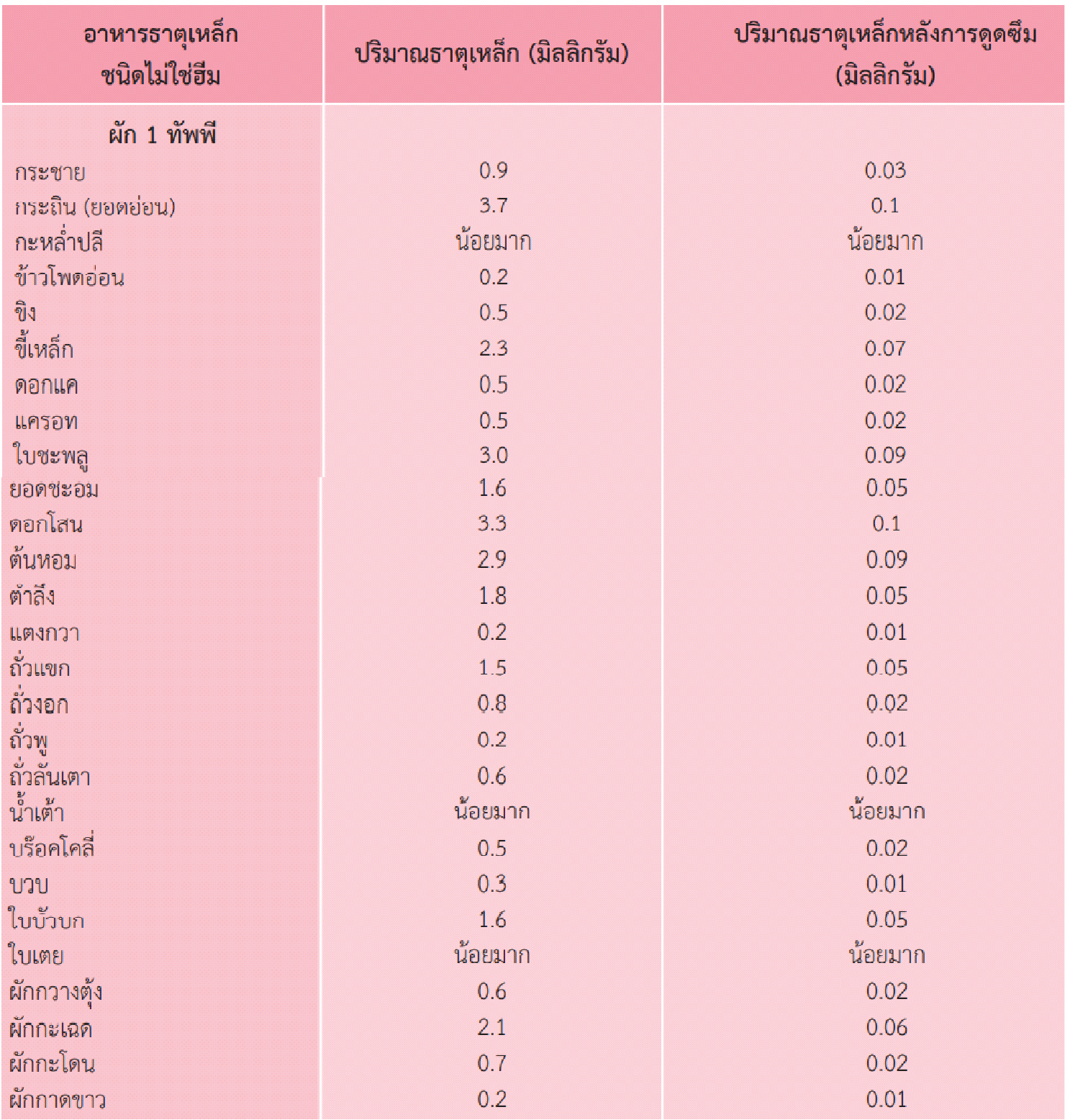
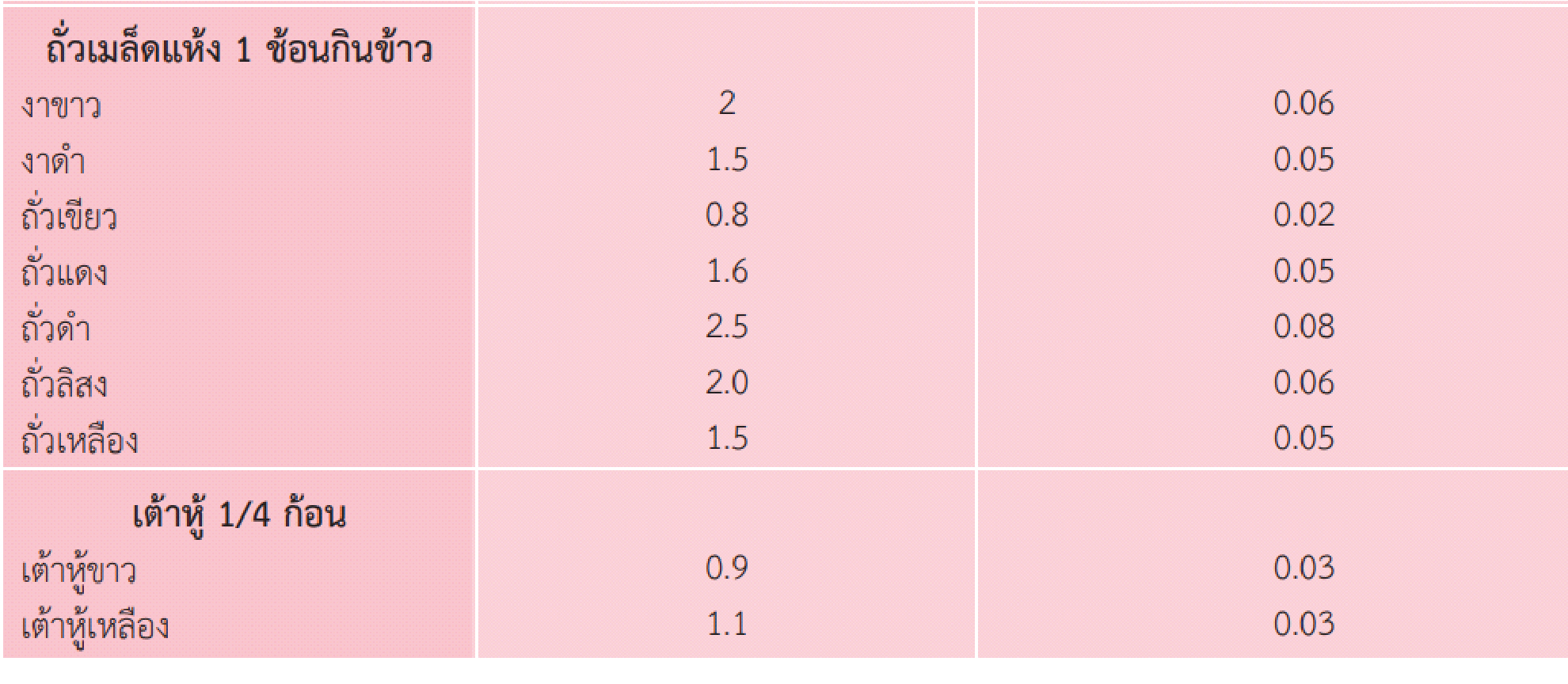
ปริมาณที่ควรได้รับธาตุเหล็ก
ในภาวะปกติ ร่างกายจะมีความต้องการธาตุเหล็กประมาณ 20 ถึง 25 มิลลิกรัมต่อวัน ซึ่งส่วนใหญ่จะถูกนำไปใช้ในการสังเคราะห์ฮีโมโกลบิน โดยแหล่งหลัก ได้แก่ ม้าม ซึ่งทำหน้าที่สลาย ฮีโมโกลบินในเม็ดเลือดแดงที่หมดอายุ และปลดปล่อยเหล็กในโมเลกุลฮีโมโกลบินกลับเข้าสู่กระแสเลือด เพื่อให้ร่างกายสามารถนำกลับไปใช้ประโยชน์ได้อีก แต่อย่างไรก็ตามความต้องการใช้ธาตุเหล็ก ในแต่ละวันซึ่งมีรายละเอียดตามตารางต่อไปนี้
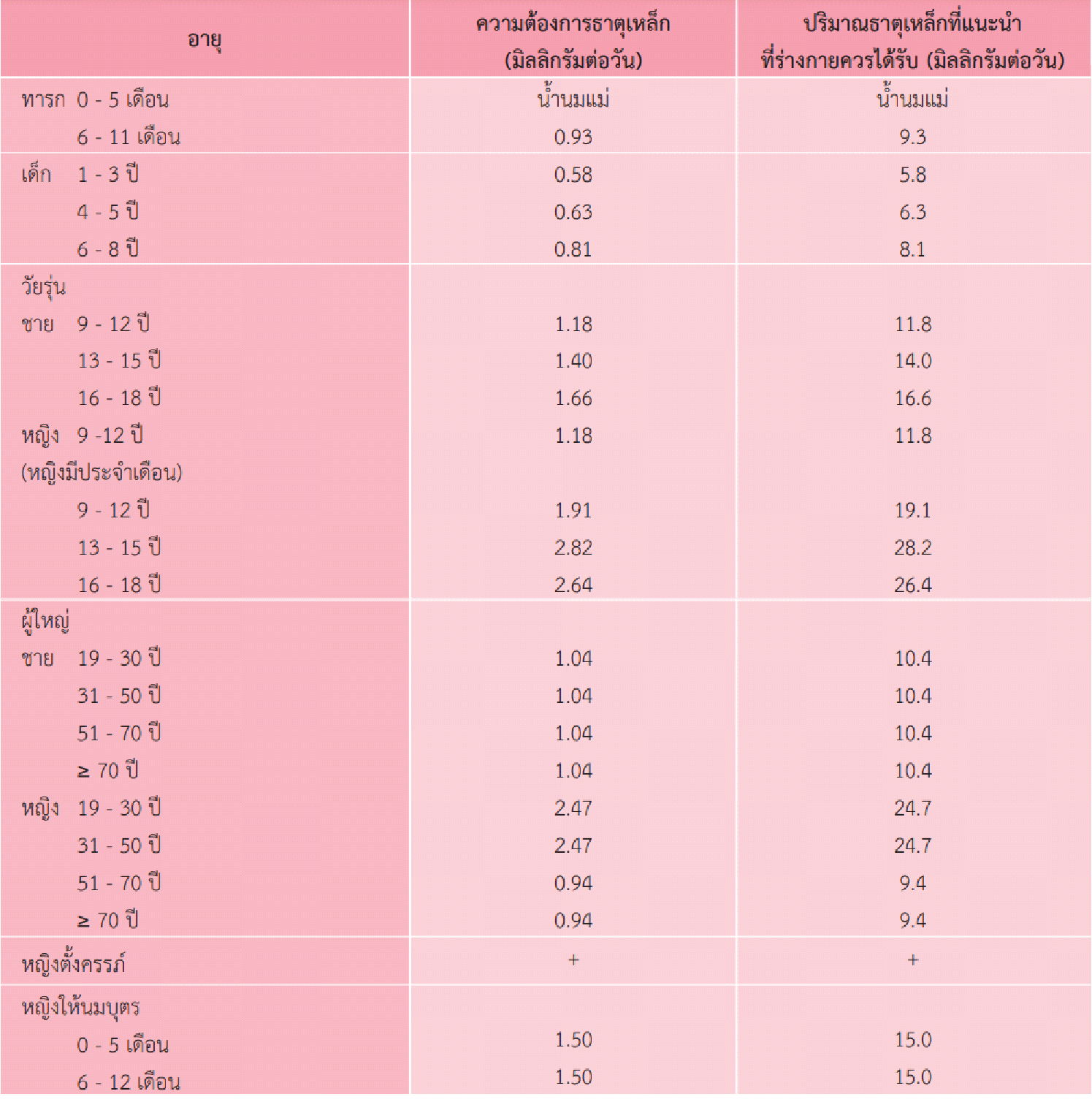
ที่มา : ปริมาณสารอาหารอ้างอิงที่ควรได้รับประจำวันสำหรับคนไทย คณะกรรมการจัดทำข้อกำหนดสารอาหารที่ควรได้รับประจำวันสำหรับคนไทย 2546
- ความต้องการธาตุเหล็ก หมายถึง ค่าความต้องการธาตุเหล็กของร่างกายในกลุ่มอายุต่างๆ ซึ่งขึ้นอยู่กับการสูญเสียธาตุเหล็ก หรือ ความต้องการธาตุเหล็กที่เพิ่มขึ้นจากภาวะทางสรีรวิทยาของร่างกาย ได้แก่ การสูญเสียประจำวัน การสูญเสียประจำเดือน การเจริญเติบโต และการตั้งครรภ์ เป็นต้น
- ปริมาณธาตุเหล็กที่แนะนำที่ร่างกายควรได้รับ หมายถึง การกำหนดการบริโภคธาตุเหล็กจากแหล่งอาหารที่ควรได้รับประจำวันซึ่งใช้ค่า bioavailability ที่ร้อยละ 10
- ไม่มีการกำหนดค่าความต้องการธาตุเหล็ก เนื่องจากมีความต้องการสูงเกินกว่าธาตุเหล็ก ที่ได้รับจากอาหารประจำวัน มีความจำเป็นต้องได้รับการเสริมธาตุเหล็กทุกวันในปริมาณวันละ 60 มิลลิกรัม และยังคงมีข้อแนะนำในเรื่องอาหาร เช่นเดียวกับหญิงที่ไม่ได้ตั้งครรภ์
ประโยชน์และโทษธาตุเหล็ก
ธาตุเหล็กมีหน้าที่สำคัญในร่างกายมนุษย์ คือ เป็นส่วนสำคัญในการสร้างเม็ดเลือดแดงโดยธาตุเหล็กจะอยู่ที่เม็ดเลือดแดงในรูปของฮีโมโกลบิน และเก็บสะสมอยู่ที่ตับ และม้าม จากนั้นจะออกมาอยู่ในกระแสเลือดทำหน้าที่นำออกซิเจนไปยังปอด และเซลล์เนื้อเยื่อต่างๆ ซึ่งเม็ดเลือดแดงจะมีอายุประมาณ 120 วัน หลังจากนั้นเม็ดเลือดแดงจะถูกทำลาย และธาตุเหล็กจะถูกปล่อยออกมา และนำกลับไปใช้ใหม่ในการสร้างฮีโมโกลบิน และสร้างเม็ดเลือดแดงใหม่อีกครั้ง อีกทั้งธาตุเหล็กยังมีความสำคัญกับร่างกายมนุษย์ในแต่ละช่วงวัย เช่น
กลุ่มหญิงตั้งครรภ์ และทารก สำหรับหญิงตั้งครรภ์ที่มีภาวะโลหิตจากจากการขาดธาตุเหล็ก จะมีภาวะเสี่ยงต่อการคลอดก่อนกำหนด และหากเสียเลือดมากในการคลอด อาจเป็นอันตรายถึงชีวิต ซึ่งเด็กทารกที่คลอดก่อนกำหนดก็จะมีน้ำหนักต่ำกว่าเกณฑ์ และมีธาตุเหล็กสะสมน้อย
กลุ่มเด็กปฐมวัยและเด็กวัยเรียน ธาตุเหล็กมีความสำคัญต่อการเจริญเติบโตทางด้านร่ายกาย และมีผลต่อพัฒนาการทางสมอง สติปัญญา ส่วนในเด็กที่มีภาวะโลหิตจางจากการขาดธาตุเหล็กนั้น ส่งผลเสียต่อศักยภาพการเรียนรู้ ทำให้เด็กไม่สามารถเรียนรู้และมีพัฒนาการได้เท่ากับเด็กปกติ
กลุ่มหญิงวัยเจริญพันธุ์ ในหญิงที่เข้าสู่วัยเจริญพันธุ์ และมีประจำเดือน จะสูญเสียธาตุเหล็ก จากการมีประจำเดือน ดังนั้นธาตุเหล็กมีความสำคัญต่อหญิงวัยเจริญพันธุ์ ถ้าหญิงวัยเจริญพันธุ์มีภาวะโลหิตจางจากการขาดธาตุเหล็กจะทำให้ประสิทธิภาพในการเรียนหรือการทำงานลดลง และอาจมีผลกระทบสำหรับการตั้งครรภ์ในอนาคตได้
กลุ่มผู้ใหญ่ ธาตุเหล็กมีความสำคัญต่อการพัฒนะศักยภาพด้านสมรรถภาพในการทำงาน ในวัยผู้ใหญ่ทั้งหญิง และชาย หากผู้ใหญ่มีภาวะโลหิตจางจากการขาดธาตุเหล็ก ก็จะทำให้ประสิทธิภาพในการทำงานลดลง อ่อนเพลีย เหนื่อยง่าย จนมีผลกระทบกับหน้าที่การงานได้
นอกจากนี้หากมีภาวการณ์ขาดธาตุเหล็กอาจทำให้การเจริญเติบโตของเซลล์ต่างๆ จะเกิดภาวะผิดปกติได้ เช่น เซลล์เม็ดเลือดแดง มีฮีโมโกลบินลดลง มีการนำ และสะสมออกซิเจนลดลง ทำให้ซีด อ่อนล้าง่าย เซลล์เยื่อบุทางเดินอาหาร ภาวะขาดธาตุเหล็กอย่างรุนแรง อาจทำให้ลิ้นเลี่ยน เยื่อบุหลอดอาหาร กระเพาะอาหาร ลำไส้เรียบบาง ทำให้น้ำย่อยลดลง การย่อย และการดูดซึมอาหารลดลง การเจริญเติบโตช้าลง ความสามารถในการทำงานของกล้ามเนื้อลดลง เนื่องจากภาวะขาดธาตุเหล็กทำให้ไมโอโกลบินลดลง
ส่วนในปัจจุบันมีการผลิตยา หรือ ผลิตภัณฑ์เสริมธาตุเหล็ก มาใช้ในทางการแพทย์ และวงการอาหารเสริมเพื่อสุขภาพ เพื่อให้ผู้ที่มีภาวะเสี่ยงต่อการขาดธาตุเหล็กได้รับประทานเสริมจากมื้ออาหาร แต่ก็มีรายงานการพบอาหารไม่พึงประสงค์จากการรับประทานธาตุเหล็ก ได้แก่ มีอาการคลื่นไส้อาเจียน ท้องเสีย หรือท้องผูก ดังนั้นทางการแพทย์จึงมีข้อแนะนำในการรับประทานซึ่งหากมีอาการข้างเคียงเหล่านี้อาจรับประทานธาตุเหล็ก พร้อม หรือ หลังมื้ออาหารทันที แต่หากอาการข้างเคียงไม่ลดลงควรปรึกษาแพทย์ทันที
การศึกษาวิจัยที่เกี่ยวข้องธาตุเหล็ก
มีผลการศึกษาวิจัยระบบดูดซึมธาตุเหล็กของร่างกายจากอาหารที่รับประทานเข้าไปพบว่า ธาตุเหล็กในอาหารอยู่ในรูปของ heme (ได้แก่ เหล็กที่อยู่ในเลือดเนื้อสัตว์) หรือ non-heme (เหล็กที่อยู่เป็น inorganic form หรือ อย่างอื่น ได้แก่ เหล็กที่อยู่ในพืชทั้งหมด เช่น ข้าว ถั่วเมล็ด รวมทั้งในไข่แดง และนม) ร่างกายจะมีระบบการดูดซึมผ่านลำไส้ที่แตกต่างกัน โดยในรูปของ heme สามารถถูกดูดซึมเข้าไปโดยตรง โดยอาศัย heme iron transporter (HCP1) ที่ควบคุมโดยปัจจัย เช่น การขาดเหล็ก หรือ hypoxia ส่วนเหล็กในรูป non-heme ในอาหารที่รับประทานต้องถูกเปลี่ยนให้อยู่ในรูปของ ferric iron ในลำไส้ ดังนั้นจึงต้องเปลี่ยนกลับให้เป็น ferrous โดยอาศัย enzyme พวก ferric reductase ได้แก่ duodenal cytochrome b (DCYTB) ที่ brush border หรือ วิตามินซี ที่อยู่ในอาหารที่รับประทานในมื้อเดียวกันนั้น จากนั้นเหล็กจะอาศัย HCP1 นำเข้าสู่ enterocyte แล้วถูกส่งต่อเข้าสู่ระบบหมุนเวียนโดยโปรตีน Ferroportin1 และมี hephaestin และ ceruloplasmin ซึ่งเป็น oxidaseenzyme ในการช่วยให้เหล็กสามารถผ่านผนังของ enterocyte และ macrophage ตามลำดับ และการดูดซึมธาตุเหล็กในรูป non-heme iron จากอาหารยังขึ้นอยู่กับชนิด และปริมาณของสารอื่นที่อยู่ในอาหารที่ช่วยเสริม (absorption enhancer) หรือ ขัดขวางการดูดซึม (absorption inhibitor) วิตามินซี กรดอะมิดน และเปปไทด์จากโปรตีนจากเนื้อสัตว์ และกรดอินทรีย์ในพืชผัก ผลไม้ ช่วยเสริมการดูดซึม ในขณะที่อาหารที่มีส่วนประกอบของ phytate และสาร polyphenols ขัดขวางการดูดซึม ข้าวที่ไม่ขัดสี หรือ ขัดสีเพียงเล็กน้อย มักมีปริมาณของ phytate สูง ถั่วเมล็ดแห้ง เช่น ถั่วเหลืองมีทั้ง non-heme iron และ phytate สูง ปักใบเขียวที่มีสีเข้ม พริกขมิ้น มี polyphenols ในเกณฑ์สูง นอกจากนี้ยังพบว่า การรับประทานนมในมื้อเดียวกับอาหารที่มีเหล็กในรูปของ non-heme ยังมีผลขัดขวางการดูดซึมได้ด้วย ทั้งนี้ธาตุเหล็ก ที่ใช้เสริมในนมผง หรือ อาหารต่างๆ ในอุตสาหกรรมก็มักเป็นสารประกอบที่เป็น non-heme iron เช่นกัน
เหล็กส่วนที่ไม่ถูกนำเข้าเซลล์จะเก็บสะสมในรูปของ ferritin ที่ผนังลำไส้ และหลุดลอกออกตามปกติ นอกจากนี้ยังพบว่าฮอร์โมนที่มีบทบาทสำคัญในการควบคุม การดูดซึมธาตุเหล็กจากอาหาร และการทำงานของ macrophage คือ hepcidin ซึ่งเป็นโปรตีนซึ่งถูกสังเคราะห์ที่เซลล์ตับเป็นหลัก โดยอยู่ภายใต้อิทธิพลของปัจจัยต่างๆ ปริมาณเหล็กในร่างกาย : ปริมาณเหล็กในร่างกายที่เพิ่มสูงขึ้นจะกระตุ้นการสังเคราะห์ hepcidin โดยเซลล์ตับสามารถรับรู้ปริมาณเหล็กในพลาสมาในรูปของ diferric transferrin และ transferrin saturation ผ่านทางกลไกซึ่งต้องอาศัยการทำงานของโปรตีนหลายชนิด การทำงานของไขกระดูกในการสังเคราะห์เม็ดเลือดแดง ในภาวะที่ไขกระดูกมีการสังเคราะห์เม็ดเลือดแดงเพิ่มขึ้น ตับจะลดการสังเคราะห์ hepcidin นอกจากระดับการสังเคราะห์เม็ดเลือดแดงของไขกระดูกแล้ว ภาวะ ineffective erythropoiesis ยังมีอิทธิพลกดการสังเคราะห์ hepcidin เช่นเดียวกัน การอับเสบ การสังเคราะห์ hepcidin จะได้รับการกระตุ้นในภาวะที่ร่างกายมีการอักเสบ ทั้งนี้เป็นผลจากฤทธิ์ของ cytokine โดยเฉพาะอย่างยิ่ง IL-6 ซึ่งทำหน้าที่เป็นกลไกหลักในการเหนี่ยว - นำการสังเคราะห์ hepcidin ผ่านทาง JAK-STAT pathway โดยทำงานเป็นอิสระจากกลไกควบคุม hepcidin ของปริมาณเหล็กในร่างกาย นอกจาก IL-6 แล้ว cytokine ชนิดอื่นๆ อาจมีบทบาทควบคุม การสังเคราะห์ hepcidin
จากการที่ hepcidin และกลไกควบคุมสมดุลเหล็กในระดับร่างกาย อยู่ภายใต้อิทธิพลของ ปัจจัยกลุ่มเดียวกัน โดยระดับการสังเคราะห์ hepcidin มีความสัมพันธ์ในเชิงปฏิภาคกับปริมาณเหล็ก ที่ผ่านเข้าสู่พลาสมา ทำให้เชื่อว่า hepcidin อาจทำหน้าที่เป็นตัวจักรสำคัญในกลไกดังกล่าว ซึ่งได้รับการพิสูจน์โดยการศึกษาการออกฤทธิ์ของ hepcidin ที่พบว่า hepcidin มีหน้าที่ลดปริมาณ เหล็กในพลาสมาโดยยับยั้งการดูดซึมเหล็กที่ลำไส้เล็ก ตลอดจนการปลดปล่อยเหล็กจากม้ามกลับสู่ กระแสโลหิต ผลการศึกษากลไกการทำงานของ hepcidin บ่งชี้ว่า hepcidin สามารถลด การขนส่งเหล็กออกจากเซลล์ได้ โดยการเหนี่ยวนำให้เกิดการเคลื่อนย้ายโปรตีน ferroportin เข้าสู่ ไซโตพลาสม ก่อนที่จะถูกย่อยสลายที่ไลโซโซมโดยผ่านขบวนการ ubiquitination
ข้อแนะนำและข้อควรปฏิบัติ
- ผู้ป่วยโรคธาลัสซีเมียที่มีระดับความรุนแรงของโรคปานกลาง และรุนแรงมาก ควรหลีกเลี่ยงการรับประทานยาเม็ดเสริมธาตุเหล็ก รวมถึงอาหารที่มีธาตุเหล็ก
- สตรีมีครรภ์, สตรีให้นมบุตร ทารก เด็กก่อนวัยเรียน สตรีวัยรุ่น-วัยเจริญพันธุ์ เป็นกลุ่มบุคคลที่เสี่ยงต่อการเกิดภาวะขาดธาตุเหล็ก ดังนั้นการรับประทานอาหารที่เป็นแหล่งของธาตุเหล็ก โดยเฉพาะ (heme)
- มีรายงานว่าการรับประทานธาตุเหล็กมากเกินไปอาจก่อนให้เกิดอนุมูลอิสระในร่างกาย ซึ่งอาจส่งผลเสียต่อเซลล์ต่างๆ ได้ ดังนั้นจึงควรรับประทานตามแพทย์สั่งอย่างเคร่งครัด
เอกสารอ้างอิง ธาตุเหล็ก
- พัตธนี วินิจจะกูล บทบาทของธาตุเหล็ก ต่อปัญหาโลหิตจางในประเทศกำลังพัฒนา, วารสารโลหิตวิทยาและเวชศาสตร์บิรการโลหิต, 2551; 18(4)321-328.
- ธนนท์ ศุข.ธาตุเหล็ก พัฒนาสมองพัฒนาชีวิต. คอลัมน์ เรื่องเด่นจากปก : นิตยสารหมอชาวบ้าน เล่มที่ 298. กุมภาพันธ์ 2547
- กอบโภชนาการ กรมอนามัย กระทรวงสาธารณสุข,ตำหรับอาหารที่อุดมด้วยธาตุเหล็ก 254;8-42, พิมพ์ครั้งที่ 2, โรงพิมพ์องค์การสงเคราะห์ทหารผ่านศึก
- คณะกรรมการจัดทำข้อกำหนดสารอาหารที่ควรได้รับประจำวันสำหรับคนไทย กองโภชนาการ กรมอนามัย กระทรวงสาธารณสุข,แร่ธาตุที่ร่างกายต้องการปริมาณน้อย, ธาตุเหล็ก ปริมาณสารอาหารอ้างอิงที่ควรได้รับสำหรับคนไทย, 2546, 249-258, พิมพ์ครั้งที่ 1, โรงพิมพ์องค์การรับส่งสินค้า และพัสดุภัณฑ์
- รศ.ดร.ภญ.บุษบา จินดาวิจักษณ์. การใช้ธาตุเหล็กแก่ภาวะโลหิตจาง. บทความเผยแพร่ความรู้สู่ประชาชน. คณะเภสัชศาสตร์มหาวิทยาลัยมหิดล.
- กองโภชนาการ กรมอนามัย กระทรวงสาธารณสุข, ตารางแสดงคุณค่าทางโภชนาการของอาหารไทย, 2544 ; 9-77. พิมพ์ครั้งที่ 2.โรงพิมพ์องค์การทหารผ่านศึก
- คู่มือแนวทางการควบคุมและป้องกันโลหิตจางจากการขาดธาตุเหล็ก. สำนักโภชนาการกรมอนามัย กระทรวงสาธารณสุข. 56 หน้า
- พัตธนี วินิจจะกูล.ธาตุเหล็ก และการนำไปใช้ประโยชน์ในร่างกาย. วารสารโภชนาการ ปีที่ 52. ฉบับที่ 1 มกราคม-มิถุนายน 2560. 38 หน้า
- Vulpe CD, Kuo YM, Murphy T, Cowley L, Askwith C. Hephaestin, a ceruloplasminhomologue implicated in intestinal iron transport, is defective in the SLA mouse. Nat Genet 21: 1999; 195-9
- De Domenico I, Ward DM, Langelier C, Vaughn MB, Nemeth E, Sundquist WI, et al. The molecular mechanism of hepcidin-mediated ferroportin down-regulation. Mol Biol Cell 2007;18(7):2569-78.
- Monsen ER, Hallberg L, Layrisse M, Hegsted DM, Cook JD, Mertz W, Finch CA. Estimation of available dietary iron. Am J Clin Nutr 1978; 31: 134-141.
- Beard JL, Dawson H, Pinero DJ. Iron metabolism: A comprehensive review.Nutr Rev 1996:295-317.
- Zimmermann MB, Zeder C Muthayya S, Winichagoon P, Chaouki N, Hurrell RF. Adiposity in women and children from transition countries predicts decreased iron absorption, iron deficiency and a reduced response to iron fortification. Int J Obesity 2008; 32(7): 1098-104.
- Tanno T, Bhanu NV, Oneal PA, Goh SH, Staker P, Lee YT, et al. High levels of GDF15 in thalassemia suppress expression of the iron regulatory protein hepcidin. Nat Med 2007;13(9):1096-101.
- Hellman NE, Gitlin JD. Ceruloplasmin metabolism and function. Annu Rev Nutr 2002; 22: 439-58
- Tolkien Z, Stecher L, Mander AP, Pereira DI, Powell JJ. Ferrous sulfate supplementation causes significant gastrointestinal side-effects in adults: a systematic review and meta-analysis. PLoS One. 2015;10(2):e0117383.
- Nemeth E, Tuttle MS, Powelson J, Vaughn MB, Donovan A, Ward DM, et al. Hepcidin regulates cellular iron efflux by binding to ferroportin and inducing its internalization. Science 2004;306(5704):2090
- Zimmermann M. Nutritional iron deficiency. Lancet 2007;370: 511-20
- Hallberg L. Bioavailability of iron in man. Ann Rev Nutr 1981: 123-47.
- Lynch, S. Iron Metabolism. In: Nutritional Anemia. K. Kraemerand Zimmermann, Z (eds). Sight & Life Press, Bazel, Switzerland, 2007. Chapter 6.
- Wrighting DM, Andrews NC. Interleukin-6 induces hepcidin expression through STAT3. Blood 2006;108(9):3204-9.
- Boontaveevywat N, Kwanbunchan S, The heme iron content of urban and rural Thai diets. J Med Assoc Thai 2001: 1131-6.
- Taher AT, Saliba AN. Iron overload in thalassemia: different organs at different rates. Hematology Am Soc Hematol Educ Program. 2017;2017(1):265-71.