โครเมียม
โครเมียม
ชื่อสามัญ Chromiun
ประเภทและข้อแตกต่างโครเมียม
โครเมียมเป็นธาตุชนิดหนึ่งในตารางธาตุที่มีสัญลักษณ์ Cr. และมีหมายเลขอะตอม 24 เป็นธาตุโลหะทรานซิตัน (Transution metal) ในบล็อก D ซึ่งชื่อของโครเมียมนี้รากศัพท์มาจากภาษากรีกว่า Crome ที่หมายถึงสีสำหรับหน้าที่ของธาตุโครเมียมที่เกี่ยวข้องกับระบบร่างกายของมนุษย์นั้น อาจกล่าวได้ว่าโครเมียม เป็นแร่ธาตุชนิดหนึ่งที่ร่างกายต้องการในปริมาณที่น้อยแต่ก็มีความจำเป็นต่อร่างกายเพื่อการเจริญเติบโต และสุขภาพที่ดี ซึ่งมีส่วนสำคัญอย่างยิ่งในกระบวนการเผาผลาญน้ำตาลกลูโคส คาร์โบไฮเดรต และไขมัน เพื่อให้ได้พลังงานไปหล่อเลี้ยงส่วนต่างๆในร่างกาย รวมถึงหน้าที่ที่สำคัญอื่นๆอีกมากมาย
ส่วนประเภทของโครเมียม นั้น หากแบ่งตาม Valence จะสามารถแบ่งเป็น 6 กลุ่ม (valence) คือ จำนวนอิเล็กตรอนในอะตอมที่สามารถสร้างพันธุเคมีกับธาตุอื่น) ได้แก่ โลหะโครเมียม (Cr0,Cr(0)) โมโนวาเลนต์โครเมียม (Cr+,Cr(I)) ไดวาเลนต์โคเมียม (Cr2+,Cr(II)) ไตรวาเลนต์โครเมียม (Cr3+,Cr(III)) เต็ตตระวาเลนต์โครเมียม (Cr4+,Cr(IV)) เฮกซะวาเลนต์โครเมียม (Cr6+,Cr(VI)) โดยโครเมียมที่พบตามธรรมชาติส่วนใหญ่อยู่ในรูปไตรวาเลนต์โครเมียม ซึ่งไตรวาเลนต์โครเมียมนี้เองที่เป็นธาตุที่มีความจำเป็นต่อร่างกาย
นอกจากยังสามารถแบ่งโครเมียมออกเป็นกลุ่มตามคุณสมบัติทางเคมีได้อีก เช่น chromium metal และ alloy กลุ่มนี้จะรวมถึงเหล็กกล้าไร้สนิม (stainless steel) และ chromium containing-alloy โดยทั่วไปกลุ่มนี้จะมีความเป็นพิษค่อนข้างต่ำเมื่อเทียบกับกลุ่มอื่น divalent chromium compound (Cr2+) หรือ chromous compoundsได้แก่ chromous chloride (CrCl2) และ chromous sulfate (CrSO4) กลุ่มนี้จะมีความเป็นพิษน้อย trivalent chromium compound (Cr3+) หรือ chromic compound เป็นที่ทราบกันว่า trivalent chromium เป็นธาตุที่มีความจำเป็นต่อร่างกายในขบวนการ glucose metabloism ส่วน compound อื่นๆ ที่พบในกลุ่มนี้ ได้แก่ chromic oxide (Cr2O3), chromic sulfate (Cr2[SO4]3), chromic chloride (CrCl3), chromic potassium sulfate (KCr[SO4]2) และ chromite ore (FeOCr2O3) hexavalent chromium copound (Cr6+) ซึ่งแบ่งได้เป็น 2 กลุ่มย่อย คือ
- กลุ่มที่ละลายน้ำได้ (water-soluble hexavalent compounds) ได้แก่ chromic acid, anhydride of chromic acid, monochromate, dichromate of sodium, potassium, ammonium, cesium, rubidium และ lithium เป็นต้น
- กลุ่มที่ไม่ละลายน้ำได้ (water-insoluble hexavalent compounds) ได้แก่ zinc chromate, calcium chromate, lead chromate, barium chromate, strontium chromate และ sintered chromium trioxide เป็นต้น
แหล่งที่พบและแหล่งที่มาโครเมียม
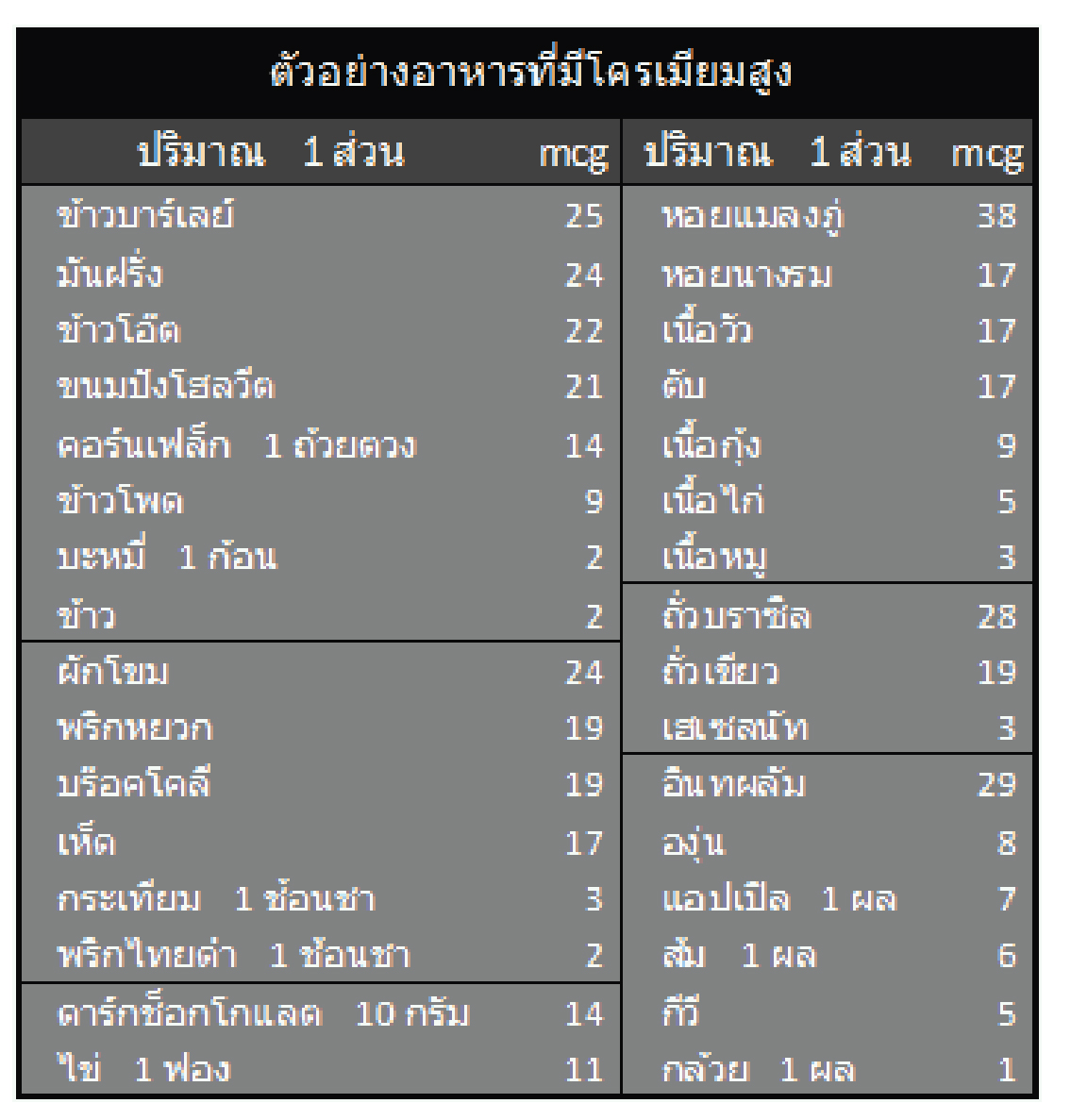
เนื่องจากโครเมียมที่ร่างกายต้องการเป็นโครเมียมที่อยู่ในรูปไตรวาเลนต์โครเมียมเท่านั้น ซึ่งแหล่งของไตรวาเลนต์โครเมียมของมนุษย์มักพบมากในแหล่งอาหารธัญพืช ข้าวกล้อง ถั่ว ถั่วเหลือง หอย ตับ เนื้อไก่ ไข่แดง เครื่องในสัตว์ เห็ด ไข่ น้ำมันข้าวโพด เนยแข็ง คาร์กช็อกโกแลต บริเวอร์ยีสต์ กากน้ำตาล ส่วนในผัก และผลไม้พบในปริมาณน้อย
นอกจากนี้ในน้ำดื่มยังพบธาตุโครเมียมได้อีกด้วย โดยระดับความเข้มข้นสูงสุดที่ยอมให้มีได้ตามเกณฑ์คุณภาพน้ำบริโภคกรมอนามัย พ.ศ.2553 และ Guideline for Drinking Water ขององค์การอนามัยโลกได้กำหนดให้มี ธาตุโครเมียม (ทุก Valence) ในน้ำไม่เกิน 0.05 มิลลิกรัมต่อลิตร ซึ่งหากมีความเข้มข้นมากกว่านี้ อาจทำให้อันตรายได้

ปริมาณที่ควรได้รับโครเมียม
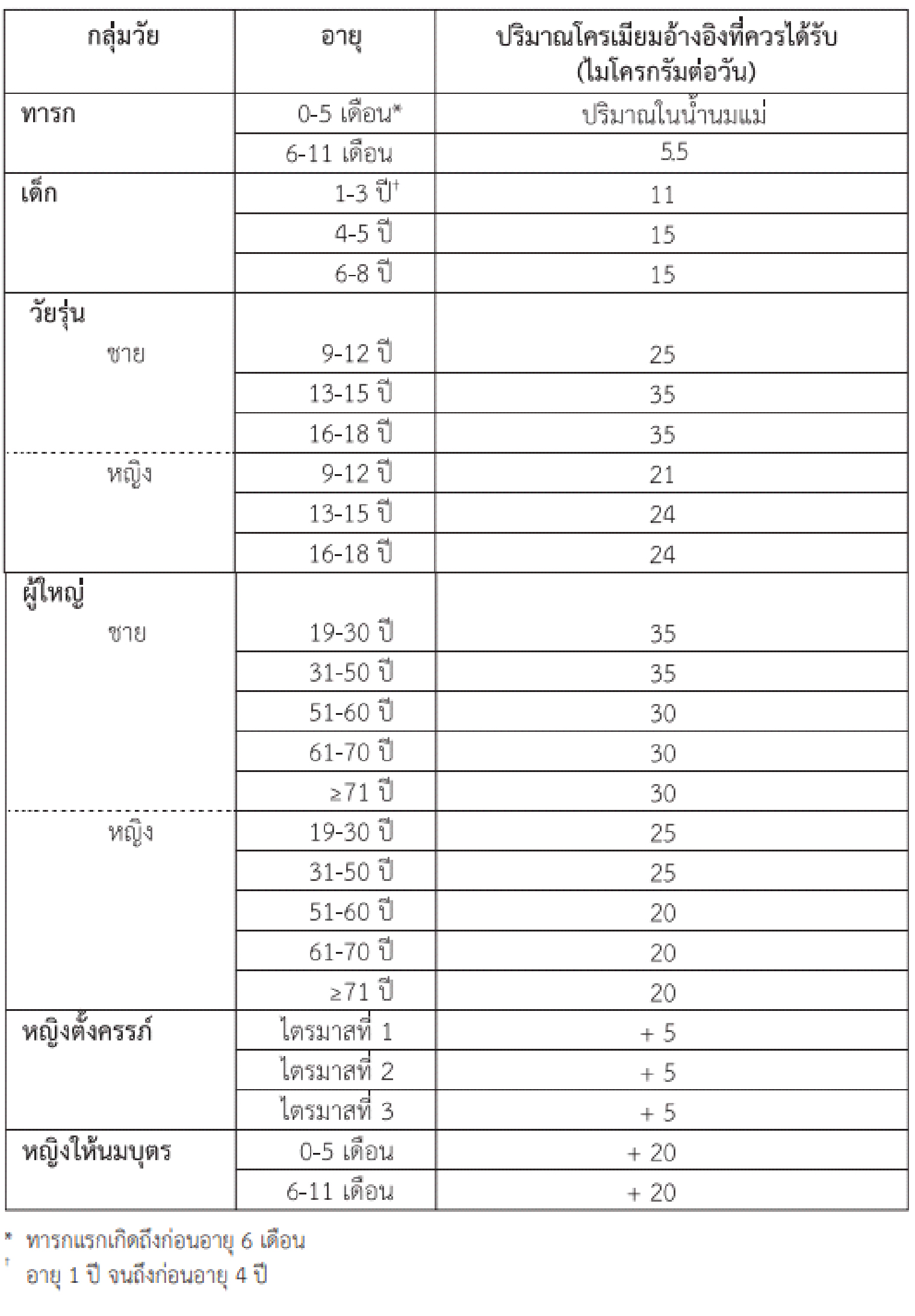
สำหรับการกำหนดปริมาณโครเมียม อ้างอิงที่ควรได้รับประจำวัน (DRI) ของไทยจะใช้ข้อมูลปริมาณอ้างอิงที่ควรได้รับประจำวัน (DRI) ของประเทศสหรัฐอเมริกาเป็นหลัก และปรับค่าตามน้ำหนักมาตรฐานของคนไทย ซึ่งจะได้ปริมาณโครเมียมอ้างอิงที่ควรได้รับประจำวันของบุคคลวัยต่างๆ ดังตาราง
ปริมาณโครเมียมอ้างอิงที่ควรได้รับประจำวันสำหรับกลุ่มบุคคลวัยต่างๆ
ประโยชน์และโทษโครเมียม
สำหรับประโยชน์ด้านสุขภาพนั้น โครเมียมกลุ่ม Trivalent chromium compound (Cr3+) หรือ chromic compound จะเป็นกลุ่มที่มีความจำ เป็นต่อร่างกาย ซึ่งจะประกอบไปด้วย chromic oxide (Cr2 O3 ), chromic sulfate (Cr2 [SO4 ] 3 ), chromic chloride (CrCl3 ), chromic potassium sulfate (KCr[SO4 ] 2 ) และ chromite ore (FeOCr2 O3) โดยจะทำหน้าที่เสริมการทำงานของฮอร์โมนอินซูลิน จากการศึกษาพบว่า chromium-binding substance ที่มีน้ำหนักโมเลกุลต่ำ มีบทบาทในเมตาบอลิสมของคาร์โบไฮเดรต และไขมันผ่านกลไกของอินซูลินซึ่งสารดังกล่าวจะจับกับ insulin receptor (IR) และจะกระตุ้นการทำงานของ insulin receptor tyrosine kinase ทำให้ inactive IR เปลี่ยนเป็น active IR และยังสามารถควบคุมระดับของปริมาณโคเรสเตอรอลในเลือดได้ โดยจะไปเพิ่มปริมาณโคเรสเตอรอลชนิด HDL (high density lipoprotein) ซึ่งเป็นชนิดที่มีประโยชน์ต่อร่างกาย และลดการสร้าง LDL (low density lipoprotein) ช่วยรักษาสมดุลของน้ำตาลในร่างกายของผู้ป่วยเบาหวาน ผู้สูงอายุ และเด็กที่ขาดสารอาหาร ส่วนโทษของโครเมียม สามารถแบ่งออกเป็น 2 ประเภท ได้แก่ ภาวะขาดโครเมียม เมื่อร่างกายได้รับโครเมียมน้อยกว่าปกติ จะทำให้ไกลโคเจนที่สะสมไว้ในร่างกายลดลงไปอย่างรวดเร็ว และทำให้อินซูลินทำหน้าที่ได้ไม่สมบูรณ์ และการเผาผลาญกรดอะมิโนมีความผิดปกติ รวมถึงระดับของคอเลสเตอรอลในเลือดจะเพิ่มขึ้นและทำให้มีอาการต่างๆ คือ ผนังเส้นเลือดเป็นแผล มีอาการคล้ายคนเป็นเบาหวาน คือ อ่อนเพลีย น้ำหนักลด ชาปลายมือปลายเท้า มีไตรกลีเซอไรด์ในเลือดสูงขึ้น แต่ HDL ลดลง มีน้ำตาลในเลือดสูงหลังอาหาร (impaired glucose tolerance แบบเดียวกับที่พบในหญิงมีครรภ์) และอีกประเภทหนึ่ง คือ ภาวะได้รับโครเมียมเกิน ในกรณีได้รับโครเมียมเกินพบ ความเป็นพิษแบบเฉียบพลัน และเรื้อรัง ซึ่งความเป็นพิษแบบเฉียบพลัน มักพบในกรณีได้รับโดยการกิน โครเมียมเฮกซาวาเลน เช่น chromic acid ทำให้เกิดการระคายเคือง ทำ ให้มีอาการคลื่นไส้ อาเจียน ปวดท้องเป็นอันตรายต่อกระเพาะอาหารและลำ ไส้ ไตวาย และเสียชีวิตได้ซึ่งปริมาณโครเมียมเฮกซาวาเลนที่ทำ ให้เสียชีวิตได้ในผู้ใหญ่ คือ 1-3 กรัม
ส่วนความเป็นพิษแบบเรื้อรัง มักพบในคนงานที่ต้องทำงานสัมผัสกับโครเมียม และสารประกอบโครเมียมเป็นเวลานานๆ สามารถแบ่งออกเป็นความเป็นพิษต่อผิวหนัง และทางเดินหายใจ มักมีสาเหตุจากการสัมผัสโครเมียมเฮกซาวาเลนเป็นระยะเวลานานๆ ทำให้เกิดแผลเรื้อรังได้ โดยบริเวณที่สัมผัสมักได้แก่ มือ และแขน ระบบทางเดินหายใจเกิดการระคายเคืองต่อเยื่อบุโพรงจมูกตาแดง น้ำตาไหล น้ำมูกไหล คัด และแสบจมูก ในกรณีที่รุนแรงอาจเกิดแผลเรื้อรังในเยื่อบุจมูกจนเกิดผนังกั้นจมูกทะลุได้ อีกลักษณะหนึ่ง คือ เป็นสารก่อให้เกิดมะเร็ง (carcinogenicity) โดยหน่วยงาน The International Agency for Research on Cancer (IARC) และ US Toxicology Program จัดโครเมียมเฮกซาวาเลนเป็น human carcinogen เพราะมีความสามารถในการละลายน้ำที่ดี ในคนงานที่ทำงานสัมผัสกับโครเมียมเฮกซาวาเลนเป็นเวลามากกว่า 30 ปีขึ้นไป จะมีความเสี่ยงสูงในการเกิดโรคมะเร็งและพบว่าเป็นโรคมะเร็งปอดมากกว่าโรคมะเร็งชนิดอื่น
การศึกษาวิจัยที่เกี่ยวข้องโครเมียม
มีผลการศึกษาเกี่ยวกับการดูดซึมของโครเมียมในร่างกายระบุว่า ในคนทั่วไปจะได้รับโครเมียมในรูป trivalent จากอาหารที่บริโภคประจำวัน 50-200 ไมโครกรัม และประมาณ 3-5% ของอาหารที่บริโภค จะถูกดูดซึมเข้าสู่ร่างกาย เมื่อโครเมียมเข้าสู่ร่างกายแล้ว trivalent chromium จะรวมกับ transferrin ใน plasma และกระจายไปทั่วร่างกาย มีเพียงส่วนน้อยที่เข้าไปในเม็ดเลือดแดง อีกทั้งโครเมียมที่ถูกดูดซึมเข้าไปแล้วสามารถเก็บสะสมได้ที่ตับ ม้าม กระดูก เนื้อเยื่อทั่วไป และจะถูกขับออกทางไต โดยมีการประมาณว่าผู้ใหญ่ที่ได้รับโครเมียมจากอาหารวันละ 30-100 ไมโครกรัม จะมีระดับโครเมียมเฉลี่ยในปัสสาวะ 2-10 ไมโครกรัม/ลิตร อีกทั้งพบว่าการดูดซึมโครเมียมจะดีขึ้นเมื่อรับประทานร่วมกับวิตามินซี (vitamin-c, aspx?M=k&G=f) วิตามิน B3 (vitamin-B3.aspx?M=k&G=f)
นอกจากนี้ยังมีการศึกษาวิจัยถึงภาวการณ์ขาดโครเมียม พบว่ามีรายงานภาวะขาดโครเมียมในผู้ป่วยหญิงที่ได้รับอาหารทั้งหมดทางหลอดเลือดดำโดยไม่ได้เสริมโครเมียมเป็นเวลานานกว่า 3 ปี โดยพบว่าน้ำหนักตัวลดลง และมีอาการชาปลายมือปลายเท้า ระดับกลูโคส และกรดไขมันอิสระในเลือดผิดปกติ เมื่อให้โครเมียม 250 ไมโครกรัมต่อวัน ในสารละลายที่ให้ทางหลอดเลือดดำเป็นเวลา 2 สัปดาห์ พบว่าเมตาบอลิสมของกลูโคสดีขึ้น และการเสริมโครเมียมได้ผลดีในคนที่มี glucose tolerance test ผิดปกติ แต่จะไม่มีผลในคนที่มี glucose tolerance test ปกติ ส่วนการศึกษาในอาสาสมัครที่มีระดับคอเลสเตอรอลมากกว่า 240 มิลลิกรัมต่อ 100 มิลลิลิตร การเสริมโครเมียม วันละ 150 ไมโครกรัม ช่วยลดระดับ total cholesterol, LDL-cholesterol และ apolipoprotein B
ส่วนการศึกษาด้านความเป็นพิษของโครเมียม ระบุว่าไม่พบพิษของ trivalent chromium จากการรับประทานอาหารทั่วไป แต่การให้ trivalent chromium แบบฉีดในขนาดที่สูงจะทำให้ผิวหนังบริเวณที่ฉีดระคายเคือง ส่วนการให้แบบเม็ด และขนาดไม่เกิน 1000 ไมโครกรัม/วัน ยังไม่มีรายงานอาการผิดปกติ เว้นแต่ในผู้ที่มีไตเสื่อม หรือ เป็นโรคตับ พบว่าจะทำให้การทำงานของตับและไตแย่ลง
ข้อแนะนำและข้อควรปฏิบัติ
- ค่าปกติของโครเมียม ในเลือดสำหรับคนทั่วไป (serum หรือ plasma) จะเท่ากับ 0.5 ไมโครกรัม/ลิตร
- ค่าปกติของโครเมียมในปัสสาวะสำหรับคนทั่วไป ไม่ควรเกิน 5 ไมโครกรัม/กรัม ของครีเอตินิน
- ถึงแม้ว่าโครเมียมเป็นธาตุที่จำเป็นต่อร่างกายแต่ร่างกายก็ต้องการในปริมาณน้อย ซึ่งการรับประทานอาหารให้ครบ 5 หมู่ ในแต่ละวัน ก็ได้รับธาตุโครเมียมเพียงพอแล้ว โดยไม่จำเป็นต้องไปรับประทานธาตุโครเมียมในรูปแบบผลิตภัณฑ์เสริมอาหาร เพราะอาจทำให้ได้รับธาตุโครเมียม มากเกินไปได้ ซึ่งอาจก่อนให้เกินอันตรายต่อสุขภาพได้
เอกสารอ้างอิง โครเมียม
- ฉันทนา ผดุงทศ. ภัยสุขภาพจากโลหะ. วารสารคลินิก, พฤศจิกายน, 2549, ฉบับที่ 263.
- คณะกรรมการ และคณะทำงานปรับปรุงข้อกำหนดสารอาหารที่ควรได้รับประจำวันสำหรับคนไทย. ปริมาณสารอาหารอ้างอิงที่ควรได้รับประจำวัน สำหรับคนไทย พ.ศ.2563.กรุงเทพมหานคร ห้างหุ้นส่วนจำกัด เอ.วี.โปรเกรสชีพ 2563
- วิระฉัตร ศรีแนน.ผลกระทบโครเมียม และสารประกอบโครเมียมต่อสุขภาพ และสิ่งแวดล้อม.วารสารกรมวิทยาศาสตร์บริการปีที่ 60. ฉบับที่ 189. พฤษภาคม 2555.หน้า 10-12
- Bacelous DG. Chromium. Clin Toxicol 1999;37:173 -94.
- Food and Nutrition Board, Institute of Medicine. Dietary Reference Intakes for vitamin A, vitaminK, arsenic, boron, chromium, copper, iodine, iron, manganese, molybdenum, nickel, silicon, vanadium, and zinc. Washington D.C.:National Academies Press, 2002.
- Agency for Toxic Substances and Disease Control. ATSR’ toxicological profiles: Chromium. Boca Raton, Florida : Lewis Publisher CRC Press, 1997.
- Lauwerys RR. Occupational Toxicology. In : Classen CD, editors. Casarette and Doull’s Toxicology. The basic science of poison. 5th ed. New York: McGraw-Hill , 1995. p.987-1010.
- Shermaierr AJ, Conner LH, Pearson KH. Semiauto- mated determination of chromium in whloe blood and serum by Zeeman eletrothermal atomic absorption spec -trometry. Clin chim acta 1985;152:123-34.
- Brandes, E. A.; Greenaway, H. T.; Stone, H. E. N. (1956). “Ductility in Chromium”. Nature. 178 (587): 587.
- American Conference of Governmental Industrial Hygienist. Chromium documentation of the biological exposure indices (BEIs), ACGIH, Cincinnati, OH, 1991, BEI-69-74.
- International Program on Chemical Safety Environ -mental Health Criteria 61: Chromium. World Health Organi zation;1988.