ไอโซฟลาโวน
ไอโซฟลาโวน
ชื่อสามัญ Isoflavone
ประเภทและข้อแตกต่างไอโซฟลาโวน
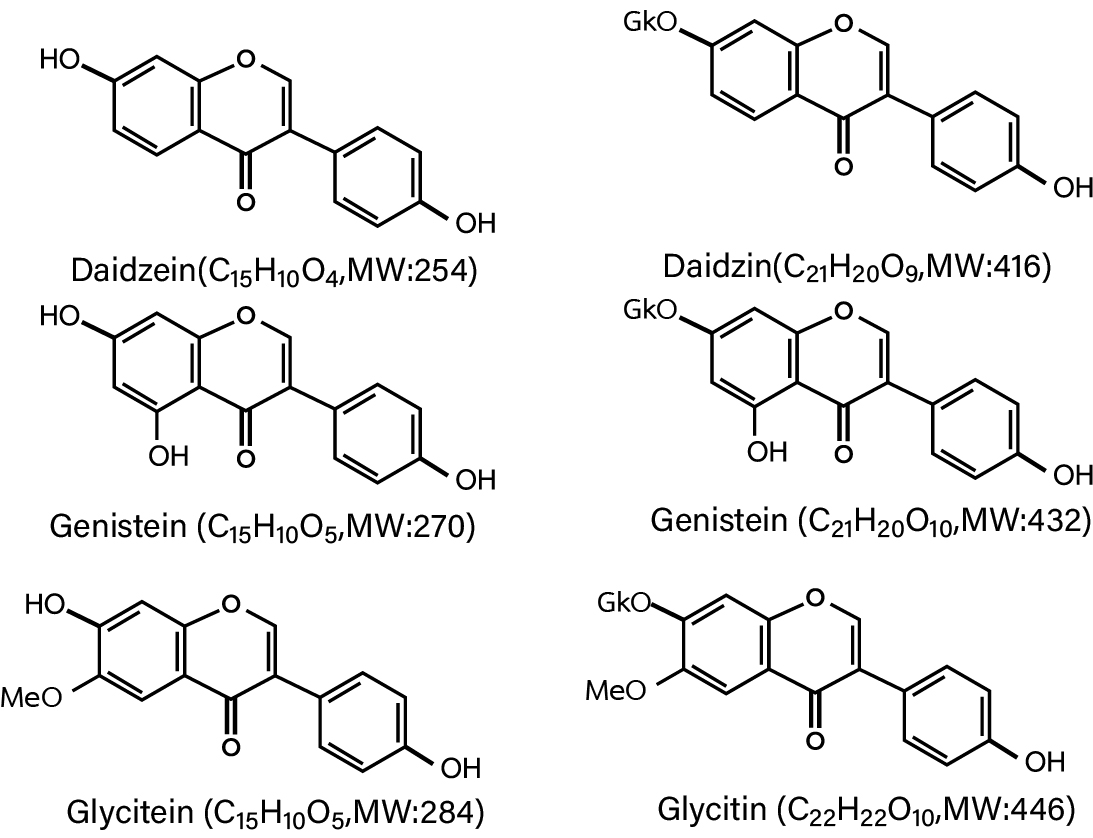
ไอโซฟลาโวน (isoflavones) จัดเป็นสารจำพวก polyphenol ที่ไม่ใช้สเตอรอยด์ (steroid) หรือ อาจเรียกว่าเป็นไฟโตนิวเทรียนต์ หรือ สารอาหารจากพืช ที่ใกล้เคียงกับฟลาโวนอยด์ โดยเป็นสารที่มีโครงสร้างพื้นฐานคลายคลึงกับของฟลาโวน (flavone) คือ ประกอบด้วย 3 วงแหวน (A, C และ B) เหมือนกัน หากแต่วงแหวน B ของไอโซฟลาโวนจะต่อกับตำแหน่งที่ 3 ของวงแหวน C แทนที่จะเป็นตำแหน่งที่ 2 เหมือนในฟลาโวน ไอโซฟลาโวน จึงจัดเป็นไอโซเมอร์ของฟลาโวน ที่เป็นสารประกอบที่มีคุณสมบัติคล้ายเอสโตรเจน สามารถจับกับ estrogen receptor และชักนำให้เกิดการตอบสนองได้เช่นเดียวกับเอสโตรเจน มักเรียกอีกชื่อว่า ไฟโตเอสโตรเจน (phytoestrogen)
สำหรับประเภทของไอโซฟลาโวนนั้นมีอยู่ด้วยกันสองรูปแบบ คือ aglycone ซึ่งเป็นไอโซฟลาโวนรูปแบบที่ไม่มีโมเลกุลของน้ำตาลมาเชื่อมต่อ โดยจะมีสามชนิด คือ daidzein genistein และ glycitein ส่วนอีกรูปแบบที่สองเป็นไอโซฟลาโวนที่มีโมเลกุลของน้ำตาลเชื่อมต่ออยู่เรียกว่า isoflavone β-glucoside ประกอบไปด้วย 6''-O-malonylglucoside 6''-O-acetylglucoside และ β-glucoside ซึ่งเกือบทั้งหมดของไอโซฟลาโวนที่พบในถั่วเหลือง จะอยู่ในรูปแบบนี้ โดยมีอัตราส่วนของ daidzein: genistein: glycitein อยู่ที่ประมาณร้อยละ 40 : 50 : 10 ของปริมาณไอโซฟลาโวนทั้งหมดที่มีอยู่ในถั่วเหลือง
แหล่งที่พบและแหล่งที่มาไอโซฟลาโวน
ไอโซฟลาโวนเป็นสารที่มีแหล่งที่มาถั่วเหลือง และผลิตภัณฑ์ที่มาจากถั่วเหลือง โดยปกติแล้วจะพบปริมาณไอโซฟลาโวน อยู่ระหว่าง 1.2-3.3 มิลลิกรัมต่อน้ำหนักแห้งของถั่วเหลืองหนึ่งกรัม ซึ่งนอกจากถั่วเหลืองแห้งแล้วผลิตภัณฑ์ที่ทำมาจากถั่วเหลืองก็มีไอโซฟลาโวนอยู่เช่นกัน ซึ่งได้แก่ เต้าหู้แผ่น, นม, ถั่วเหลือง, ถั่วเหลืองงอก, ถั่วเขียว, ถั่วขาว ถึงแม้ว่าฟองเต้าตู้ดิบ และโปรตีนถั่วเหลือง เป็นต้น นอกจากนี้ยังมีรายงานว่าพบไอโซฟลาโวน ได้จากถั่วเขียว และถั่วลันเตา อีกด้วย แต่ทั้งนี้ผลิตภัณฑ์เหล่านี้อาจมีปริมาณน้อยกว่าเมล็ดถั่วเหลืองที่ไม่ผ่านการแปรรูปมากนัก เพราะโมเลกุลของน้ำตาลที่เชื่อมต่อกับไอโซฟลาโวนที่อยู่ในรูปของ 6''-O-malonylglucoside หรือ 6''-O-acetylglucoside มีความอ่อนไหวต่อความร้อนสูง ดังนั้นหลังจากผ่านกระบวนการผลิต และแปรรูป โมเลกุลของน้ำตาลที่เชื่อมต่อกับสารไอโซฟลาโวน จะเปลี่ยมมาอยู่ในรูปของ -glucoside
นอกจากนี้กระบวนการหมักในผลิตภัณฑ์อาหารที่มาจากถั่วเหลืองบางประเภทก็ส่งผลให้น้ำตาลที่เชื่อมต่อกับโมเลกุลของไอโซฟลาโวนหลุดออกไป เป็นต้น
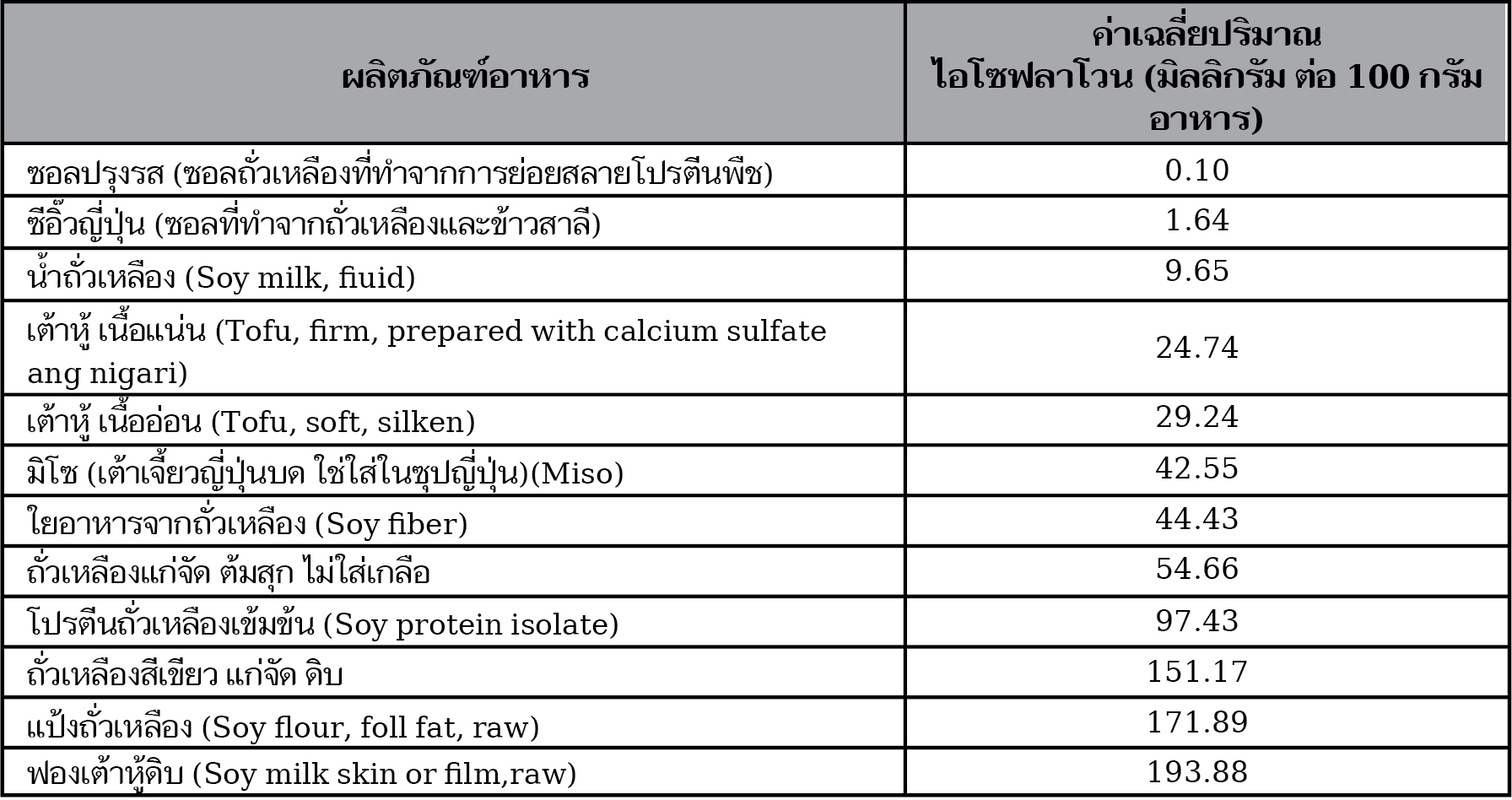
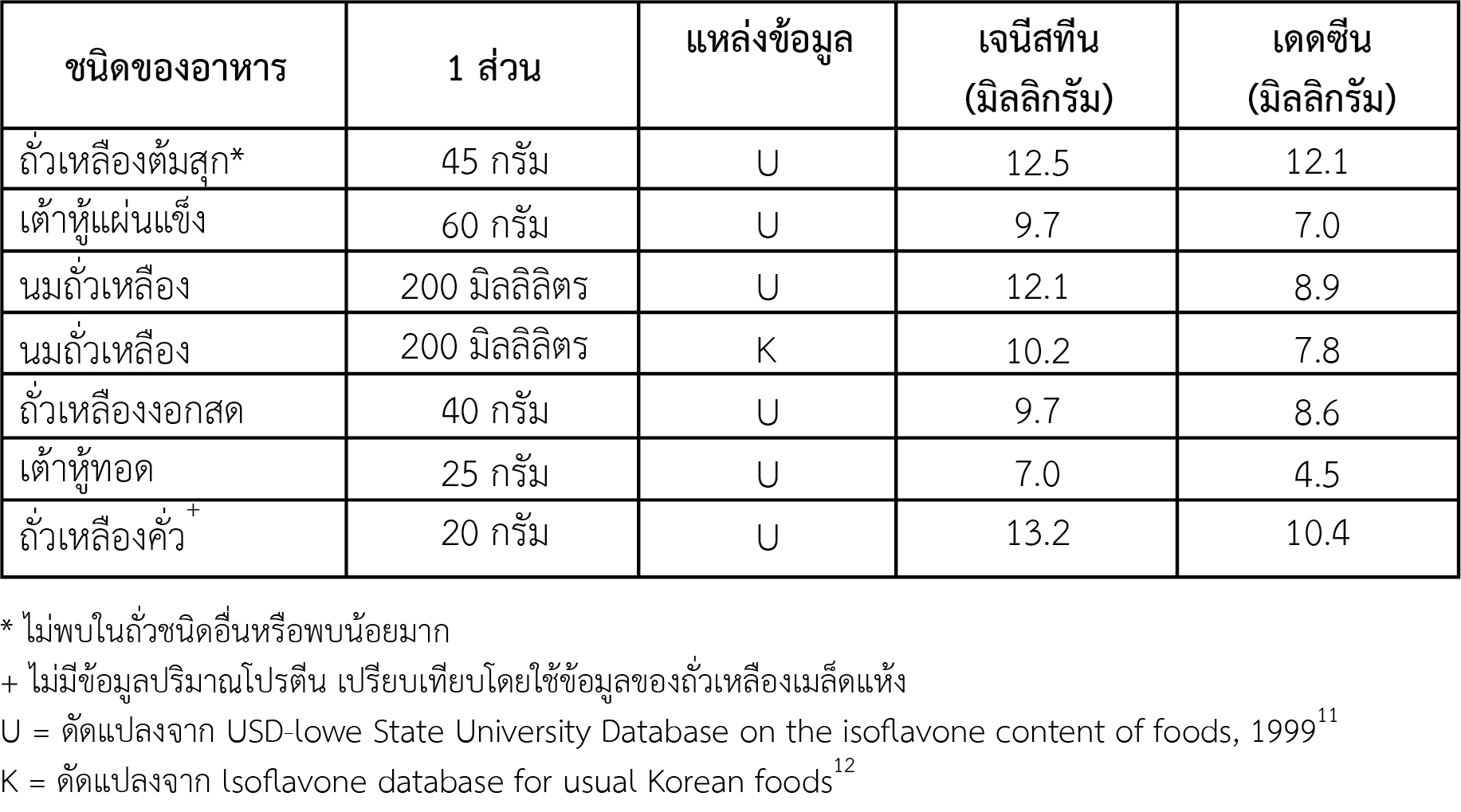
ปริมาณไอโซฟลาโวนในถั่วเหลือง และผลิตภัณฑ์จากถั่วเหลืองต่อ 1 ส่วนบริโภค

ปริมาณที่ควรได้รับจากไอโซฟลาโวน
สำหรับปริมาณของไอโซฟลาโวนที่แนะนำให้บริโภคนั้น มีการกำหนดเกณฑ์ไว้ที่ 50-100 มิลลิกรัม/วัน หรือ คิดแบบคร่าวๆ เทียบได้กับการรับประทานน้ำถั่วเหลืองประมาณวันละ 2-4 แก้ว หรือ เต้าหู้ก้อน (100 กรัม) ประมาณวันละ 2-4 ก้อน นอกจากนี้ในส่วนของสำนักงานคณะกรรมการอาหาร และยาประเทศสหรัฐอเมริกา และสมาคมแพทย์โรคหัวใจในอเมริกายังแนะนำให้รับประทานโปรตีนจากถั่วเหลือง 25 กรัมต่อวัน เพื่อให้ได้ปริมาณของโปรตีน และไอโซฟลาโวน เพียงพอใน 1 วัน
ประโยชน์และโทษไอโซฟลาโวน
เนื่องจากโครงสร้างทางเคมีของไอโซฟลาโวนมีความคล้ายคลึงกับฮอร์โมนเพศหญิง 17β-estradiol ซึ่งเป็นฮอร์โมนชนิดที่พบได้ทั่วไป และมีมากใหญ่ที่อยู่ในวัยเจริญพันธุ์ ดังนั้นสารนี้จึงถูกจัดอยู่ในกลุ่มของไฟโตเอสโตรเจน (สารที่สร้างดอกพืชซึ่งมีฤทธิ์เหมือนกับฮอร์โมนเอสโตรเจน)
ซึ่งไอโซฟลาโวน นี้สามารถจับกับ estrogen receptors และออกฤทธิ์เหมือน เอสโตรเจน (estrogen agonist) หรือ ต้านเอสโตรเจน (estrogen antagonist) คล้าย estrogen receptor modulators (SERMs) การกินถั่วเหลือง และดื่มนมถั่วเหลือง ซึ่งเป็นแหล่งของไอโซฟลาโวนเป็นประจำจะสามารถช่วยลดอาการต่างๆ ได้ เช่น อาการร้อนวูบวาบของหญิงวัยหมดประจำเดือน และโรคกระดูกพรุน อีกทั้งคุณสมบัติต้านอนุมูลอิสระของไอโซฟลาโวนจากถั่วเหลือง ยังช่วยป้องกันไม่ให้อนุมูลอิสระซึ่งเกิดขึ้นจากการเผาผลาญสารอาหารที่เราบริโภคเข้าไปทำอันตราย DNA ใน เซลล์ต่างๆ จึงช่วยลดความเสี่ยงต่อการเป็นโรคมะเร็ง ส่วนสารเจนีสทีนจะช่วยเพิ่มการสร้าง superoxide dismutase (SOD) ซึ่งช่วยกำจัดอนุมูลอิสระ นอกจากนี้ไอโซฟลาโวนจากถั่วเหลืองยังช่วยลดระดับคอเลสเตอรอลในเลือด และลด LDL-cholesterol oxidation ดังนั้นผู้ที่บริโภคถั่วเหลือง และผลิตภัณฑ์เป็นประจำจึงสามารถลดความเสี่ยงต่อการเกิดโรคหัวใจ และหลอดเลือด และโรคมะเร็งบางชนิดได้สำหรับโทษของไอโซฟลาโวนนั้นยังไม่พบรายงานแต่อย่างใด
การศึกษาวิจัยที่เกี่ยวข้องไอโซฟลาโวน
มีผลการศึกษาวิจัยเกี่ยวกับระบบการดูดซึมเข้าสู่ร่างกายของไอโซฟลาโวน โดยพบว่าขั้นตอนที่จำเป็นก่อนการดูดซึมสารไอโซฟลาโวนเข้าสู่ร่างกาย คือ การนำน้ำตาลที่เชื่อมต่ออยู่กับโมเลกุลของสารไอโซฟลาโวนออกก่อน โดยเชื่อว่าแบคทีเรียในลำไส้มีส่วนสำคัญต่อกระบวนการดังกล่าว แต่ในปัจจุบันนี้พบว่ากระบวนการดูดซึมสารไอโซฟลาโวนเกิดจากเอนไซม์ lactase phlorizin hydrolase (LPH) ในลำไส้เล็ก โดยเมื่ออยู่ในรูปของ aglycone ไอโซฟลาโวนจะซึมผ่านผนังลำไส้เล็ก ส่วนไอโซฟลาโวนที่ไม่ได้ซึมจะเคลื่อนผ่านไปยังลำไส้ใหญ่ซึ่งเป็นที่อยู่ของแบคทีเรียจำนวนมากส่งผลให้ไอโซฟลาโวนถูกย่อยด้วยเอนไซม์ของแบคทีเรียดังกล่าวเปลี่ยนเป็นอนุพันธ์ต่างๆ ก่อนที่จะเกิดการดูดซึมเข้าสู่ร่างกาย โดยdaidzein ถูกเปลี่ยนเป็น equol หรือ O-desmethylangolensin (O-DMA) ผ่านทาง dihydrodaidzein enistein ถูกเปลี่ยนเป็น 6'-hydroxy-O-DMA หรือ 5-hydroxyequol ผ่านทาง dihydrogenistein และท้ายที่สุด glycitein ถูกเปลี่ยนเป็น 5'-methoxy-O-DMA หรือ 6-methoxyequol ผ่านทาง dihydroglycitein เมื่อดูดซึมเข้าสู่ตับ ไอโซฟลาโวนจะเชื่อมต่อเข้ากับคอนดรอยตินซัลเฟล หรือ อาจเชื่อมต่อกับกรด glucuronic เพื่อเพิ่มความสามารถในการละลายน้ำของไอโซฟลาโวนหลังจากนั้นจะล่องลอยไปกับน้ำเลือด โดยไอโซฟลาโวนเมื่ออยู่ในร่างกายของมนุษย์มีค่าครึ่งชีวิต (half-life) อยู่ที่ประมาณ 7, 9 ชั่วโมง แต่ไม่มีการรายงานการศึกษาในมนุษย์ว่าหลังจากไอโซฟลาโวนถูกดูดซึมเข้าสู่กระแสโลหิตแล้วไปสะสมที่เนื้อเยื่อใดเป็นพิเศษ และจากการศึกษาทางด้านเภสัชจลนศาสตร์พบว่า ปริมาณความถี่ของการได้รับไอโซฟลาโวน อายุ เพศ และพฤติกรรมการกินไม่มีผลต่อฤทธิ์ของสารไอโซฟลาโวนในร่างกาย หากแต่เกิดจากความหลากหลายของแบคทีเรียในลำไส้ เช่น ประชากรประมาณร้อยละ 40 เท่านั้นที่มีแบคทีเรียในลำไส้ใหญ่ที่สามารถเปลี่ยน daidzein ไปเป็น equol ได้ ดังนั้นความหลากหลายของไอโซฟลาโวนที่ร่างกายได้รับไม่ได้ขึ้นอยู่กับถั่วเหลือง หรือ ผลิตภัณฑ์ที่มาจากถั่วเหลืองเพียงอย่างเดียว
นอกจากนี้ยังมีผลการศึกษาวิจัยไอโซฟลาโวน กับโรค และอาการของโรคต่างๆ ดังนี้
ภาวะหมดประจำเดือน มีการศึกษาในประเทศญี่ปุ่นพบว่า ผู้หญิงญี่ปุ่นที่รับประทานถั่วเหลืองมากทั้งในแง่ปริมาณรวมของถั่วเหลือง และไอโซฟลาโวนจะมีความถี่ของอาการร้อนวูบวาบน้อยกว่าผู้หญิงที่ไม่ได้รับประทาน และยังมีรายงานว่าผู้หญิงวัยหมดประจำเดือนในยุโรปมีอาการร้อนวูบวาบร้อยละ 70-80 ขณะที่ผู้หญิงวัยหมดประจำเดือนในมาเลเซีย จีน และสิงคโปร์มีอาการร้อนวูบวาบร้อยละ 57.18 และ 14 ตามลำดับ
โรคกระดูกพรุน ผู้หญิงหลังหมดประจำเดือนจะมีการสูญเสียเนื้อกระดูกประมาณร้อยละ 3-5 ต่อปี ในเวลา 3-5 ปีแรก ของการหมดประจำเดือน ทำให้มวลกระดูกลดลงประมาณร้อยละ 15 หลังจากนั้นอัตราการสูญเสียเนื้อกระดูก จะลดลงสู่ระดับเดิม คือ ร้อยละ 0.5-1 ต่อปีจนเข้าสู่วัยสูงอายุ ซึ่งมีรายงานการงานวิจัยพบว่าไอโซฟลาโวนจากถั่วเหลืองช่วยป้องกัน การสูญเสียมวลกระดูกได้ เนื่องจากมีคุณสมบัติคล้ายเอสโตรเจนซึ่งเพิ่มความหนาแน่นกระดูกในหญิงวัยหมด ประจำเดือน และยังมีผลการทดลองในสัตว์ทดลองที่ตัดรังไข่ออกไปนั้น พบว่าสัตว์ทดลองมีความหนาแน่นของกระดูก เนื่องจากได้รับสารไอโซฟลาโวนนี้เข้าไป เนื่องจากยังมีผลการศึกษาวิจัยพบว่าหญิงที่มีอายุตั้งแต่ 35 ปีขึ้นไปที่ยังไม่เกิดอาการของการขาดฮอร์โมนนั้น สามารถป้องกัน และหลีกเลี่ยงโรคกระดูกพรุนได้ โดยการบริโภคอาหารจากถั่วเหลืองเพื่อให้ได้สารไอโซฟลาโวน ในปริมาณวันละ 50-150 มก.
โรคมะเร็ง มีรายงานจากการทดลองศึกษาฤทธิ์การยับยั้งไลปิดเปอร์ออกซิเดชั่น (lipid peroxidation inhibition) ในตับหนู พบว่าเจนิสเคอีนจะมีฤทธิ์ในการต้านอนุมูลอิสระดีที่สุด โดยสามารถเรียงลำดับดังนี้ เจนิสเตอีนจะมีฤทธิ์ที่ดีกว่าเดดเชอีน เจนิสติน และเดดซีน ตามลำดับ นอกจากนี้ยังมีรายงานถึงฤทธิ์ของเจนิสเตอีนในการยับยั้งกระบวนการแบ่งตัวระยะไมโตเจเนซิสของเซลล์ (mitogenesis) ซึ่งเกี่ยวข้องกับการอยู่รอดของเซลล์ (cell survival) กระบวนการเปลี่ยนแปลงของเซลล์ (cell transformation) และยับยั้งขบวนการ angiogenesis ซึ่งเป็นขั้นตอนที่สำคัญที่ทำให้เกิดมะเร็งได้
โรคหัวใจขาดเลือด มีการวิเคราะห์อภิมาน (meta analysis) พบว่าการกินโปรตีนถั่วเหลืองที่มีไอโซฟลาโวนสัมพันธ์อย่างมีนัยสำคัญทางสถิติกับการลดลงของระดับ total cholesterol, LDL-cholesterol, triglycerides และการเพิ่มขึ้นของ HDL-cholesterol ทั้งนี้การเปลี่ยนแปลงของระดับไขมันในเลือดขึ้นกับเพศ ระดับเริ่มต้นของไขมัน และรูปแบบการบริโภคอาหารของกลุ่มตัวอย่าง
ส่วนอีกงานวิจัยหนึ่งพบว่าในสตรีที่มีภาวการณ์ขาดฮอร์โมนเอสโตรเจนนั้น มีโอกาสเสี่ยงต่อภาวะระดับคอเลสเตอรอลในเลือดสูง เนื่องจากคอเลสเตอรอลเป็นสารตั้งต้นตัวหนึ่งในการสร้างฮอร์โมน และเมื่อรังไข่หยุดสร้างฮอร์โมนจะมีผลทำให้มีคอเลสเตอรอลเหลือจึงส่งผลให้มีคอเลสเตอรอลในระดับสูง นอกจากนี้ยังพบว่าสารกลุ่มไอโซฟลาโวน เช่น เจนีสทีน (genistein) เป็นสารสำคัญในถั่วเหลืองที่มีผลต่อการลดของคอเลสเตอรอลชนิดดี (HDL) อีกทั้งยังช่วยป้องกันภาวะหลอดเลือดแข็งตัว และลดการจับตัวของเกล็ดเลือดที่เป็นเหตุให้เกิดภาวะการอุดตันของหลอดเลือดได้
ข้อแนะนำและข้อควรปฏิบัติไอโซฟลาโวน
⦁ สำหรับการบริโภคโปรตีนจากถั่วเหลืองเพื่อให้ได้สารไอโซฟลาโวนนั้นอาจก่อให้เกิดผลข้างเคียงน้อย และไม่รุนแรง ซึ่งโดยมากมักเป็นอาการที่เกี่ยวข้องกับระบบทางเดินอาหาร เช่น ท้องอืด แน่นท้อง ท้องผูก
⦁ ถั่วเหลืองเป็นพืชชนิดหนึ่งในตระกูลถั่ว ดังนั้นอาจมีโปรตีนบางชนิดที่ทำให้เกิดอาการแพ้โปรตีนจากถั่วได้
⦁ ในการรับประทานถั่วเหลืองเพื่อให้ได้สารไอโซฟลาโวนนั้น ควรรับประทานอาหารจากถั่วเหลืองที่มีการแปรรูปน้อยที่สุด เพราะไอโซฟลาโวนสามารถละลายน้ำได้ดี อีกทั้งหากโดนความน้อนนานๆ สารดังกล่าวอาจสูญสลายไปในปริมาณที่มาก ซึ่งอาจทำให้ร่างกายได้สารไอโซฟลาโวน ไม่เต็มที่
เอกสารอ้างอิง ไอโซฟลาโวน
⦁ ศรีวัฒนา ทรงจิตสมบูรณ์ ประโยชน์ของไฟโตเอสโตรเจน วารสารโภชนบำบัด 2544;12:8-19
⦁ จารุวรรณ ธนวิรุพัห์, ระวิวรรณ แก้วอมตะวงค์. การสกัด และแยกบริสุทธิ์สารที่มีฤทธิ์ทางชีวภาพของสารไอโซฟลาโวนในถั่วเหลือง. รายงายวิจัยฉบับสมบูรณ์ คณะเภสัชศาสตร์มหาวิทยาลัยอุบลราชธานี. 83 หน้า
⦁ รศ.วิมล ศรีศุข.ผลิตภัณฑ์ถั่วเหลืองสำหรับสตรีสตรีวัยทอง (menopause) .บทความเผยแพร่ความรู้สู่ประชาชน. คณะเภสัชศาสตร์มหาวิทยาลัยมหิดล.
⦁ พัทธินันท์ วาริชนันท์. ไอโซฟลาโวน. ไฟโตเอสโตรเจนจากถั่วเหลือง. วารสารอาหารปีที่ 45. ฉบับที่ 4 ตุลาคม-ธันวาคม 2558. หน้า 33-36
⦁ ชรินทร์ ถาวรคุโณ. ไอโซฟลาโวนจากถั่วเหลือง. ชีวเคมีกลไกการออกฤทธิ์ และความเกี่ยวข้องในการป้องกันมะเร็งเต้านม. วารสาร Thai Joumal of Genetics Vol7.No1 Jon-Apr 2014:7-15
⦁ คณะกรรมการและคณะทำงานปรับปรุงข้อกำหนดสารอาหารที่ควรได้รับประจำวันสำหรับคนไทย. ปริมาณสารอาหารอ้างอิงที่ควรได้รับประจำวัน สำหรับคนไทย พ.ศ.2563. กรุงเทพมหานคร ห้างหุ้นส่วนจำกัด เอ.วี.โปรเกรสชีพ 2563
⦁ Birt.D.F.,Frendrich.S.,and Wang W.(2001) Dietary agents in cancer prevention Flavonoids and isoflavonoids pharmacology and therapeutics Am J Cin Nutr 90.157-177.
⦁ Murphy PA, Song T, Buseman G, Barua K, Beecher GR, Trainer D, Holden J (1999) Isoflavones in retail and institutional soy foods. J Agric Food Chem 47: 2697–2704
⦁ Anderson JW, Johnstone BM, Cook-Newell ME. Meta-analysis of the effects of soy protein intake on serum lipids. N Eng J Med 1995;333:276-82.
⦁ Schoefer L, Mohan R, Braune A, Birringer M, Blaut M (2002) Anaerobic C-ring cleavage of genistein and daidzein by Eubacterium ramulus. FEMS Microbiol Lett 208: 197–202.
⦁ Wang H, Murphy PA (1994b) Isoflavone Content in Commercial Soybean Foods. J Agric Food Chem 42: 1666–1673.
⦁ Acllercreufz.H., Goldin.BR.,Gortach.SL(1995) Soybean phytoestrogen intake and cancer risk.J.Nutr.125.757s-770s.
⦁ Kudou S, Tsuizaki I, Uchida T, Okubo K (1991) Purification and some properties of soybean saponin hydrolase from Aspergillus oryzae KO-2. Agric Biol Chem 55: 31–36
⦁ U.S. Department of Agriculture. USDA-Iowa State University Database on the isoflavone content of foods. Release 1.4, April 2007. Web site: http://www.ars.usda.gov/nutrientdata.
⦁ Wei P, Liu M, Chen Y, Chen DC. Systematic review of soy isoflavone supplements on osteoporosis in women. Asian Pac J Trop Med 2012;5:243-8
⦁ Setchell KD (1998) Phytoestrogens: the biochemistry, physiology, and implications for human health of soy isoflavones. Am J Clin Nutr 68: 1333S–1346S
⦁ Zaheer K, Akhtar H. An updated review of dietary isoflavones: Nutrition, processing, bioavailability and impacts on human health. Crit Rev Food Sci Nutr 2017;57:1280-93.
⦁ Song T, Barua K, Buseman G, Murphy PA (1998) Soy isoflavone analysis: quality control and a new internal standard. Am J Clin Nutr 68: 1474S–1479S
⦁ Zava,D.,Duwe G(1997) Estrogenic and antirproliferative properties of genistein and other flavonoids in human breast cancer cells. Nutr.Cancer.27.31-40.
⦁ Day AJ, Canada FJ, Diaz JC, Kroon PA, McLauchlan R, Faulds CB, Plumb GW, Morgan MR, Williamson G (2000) Dietary flavonoid and isoflavone glycosides are hydrolysed by the lactase site of lactase phlorizin hydrolase. FEBS Lett 468: 166–170
⦁ Pawlowski JW, Martin BR, McCabe GP, McCabe L, Jackson GS, Peacock M, et al. Impact of equol-producing capacity and soy-Isoflavone profiles of supplements on bone calcium retention in postmenopausal women: a randomized crossover trial. Am J Clin Nutr 2015;102:695-703.
⦁ Nielsen IL, Williamson G (2007) Review of the factors affecting bioavailability of soy isoflavones in humans. Nutr Cancer 57: 1–10.
⦁ Park MK, Song Y, Joung H, Li SJ, Paik HY. Establishment of an isoflavone database for usual Korean foods and evaluation of isoflavone intake among Korean children. Asia Pac J Clin Nutr 2007;16:129-39.
⦁ Coward L, Smith M, Kirk M, Barnes S (1998) Chemical modification of isoflavones in soyfoods during cooking and processing. Am J Clin Nutr 68: 1486S–1491S
⦁ Bames.s (1995) Eflect genictein on In vitro and in vivo modeis of cancer.J Nutr.125.777s-783s.
⦁ Manach C, Scalbert A, Morand C, Remesy C, Jimenez L (2004) Polyphenols: food sources and bioavailability. Am J Clin Nutr 79: 727–747.
⦁ Nagata C, Takatsuka N, Kawakami N, Shimizu H. Soy product intake and hot flashes in Japanese women: results from a community-based prospective study. Am J Epidemiol 2001;153:790-3.